Methadon
Methadon ist ein vollsynthetisch hergestelltes Opioid mit starker schmerzstillender Wirksamkeit. Methadon ist reiner Agonist am μ-Opioid-Rezeptor und vermutlich am δ-Opioid-Rezeptor.[8] Es hat als Heroin-Ersatzstoff im Rahmen von Substitutionsprogrammen seine Wirksamkeit bewiesen[9] und wurde deshalb 2005 von der Weltgesundheitsorganisation (WHO) in die Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation aufgenommen.[10]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
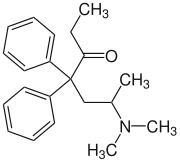
| ||||||||||||||||||||||
| Struktur ohne Stereochemie | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Methadon | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C21H27NO | |||||||||||||||||||||
| Kurzbeschreibung |
Weißes bis fast weißes, kristallines Pulver (L-Polamidon·Hydrochlorid)[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse |
| |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 309,45 g·mol−1(Methadon) | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
8,94[6] | |||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Geschichte Bearbeiten
Die später Methadon benannte Substanz wurde 1937[11] von Max Bockmühl und Gustav Ehrhart, zwei Mitarbeitern der zum I.G. Farben-Konzern gehörenden Hoechster Farbwerke, mit der Synthesenummer VA 10820 entwickelt und 1938 zum Patent angemeldet.[12][13] Die analgetische Wirkung von VA 10820 wurde 1942 in einer kleinen klinischen Studie erstmals festgestellt. Erst 1945 wurde diese Wirkung von Otto Schaumann, beziehungsweise unabhängig von ihm von Charles C. Scott und K. K. Chen,[14] beides Mitarbeiter an den Lilly Research Laboratories von Eli Lilly, definitiv nachgewiesen. Nach dem Zweiten Weltkrieg kam VA 10820 auf dem Weg der Patent- und Vorschriftenenteignung in die Vereinigten Staaten. 1947 erhielt VA 10820 den Freinamen Methadon bzw. in den USA Methadone. Im gleichen Jahr erfolgte von Eli Lilly die Markteinführung eines racemischen Methadons unter dem Markennamen Dolophine. Jede ausländische Firma konnte das Herstellungsrecht erwerben. Später wurde Methadon dann weltweit unter verschiedenen Markennamen vertrieben. Im Januar 1949 konnte die nach der Auflösung der I.G. Farben neu gegründete Hoechst AG Methadon monochiral unter der Bezeichnung L-Polamidon (Levomethadon) als stark wirkendes Schmerzmittel selbst auf den Markt bringen.[15]
Seit den 1960er Jahren wird Methadon (zuerst in den USA) als Substitutionsmittel bei Heroinabhängigkeit eingesetzt, wobei in den ersten Jahren ausschließlich mit sehr hohen Dosen in hochstrukturierten Programmen mit dem Ziel einer Dauersubstitution gearbeitet wurde – dies, weil die Opioidabhängigkeit als metabolische Störung gesehen wurde, die wie andere Stoffwechselerkrankungen auch zu behandeln sei.[16] In Deutschland wurde die Substitutionsmethode mit Dihydrocodein von dem Kieler Arzt Gorm Grimm eingeführt.[17]
Gewinnung und Darstellung Bearbeiten
Methadon wird vollsynthetisch hergestellt, im Gegensatz z. B. zu Heroin, das halbsynthetisch aus dem natürlichen Opium-Alkaloid Morphin hergestellt wird. Chemisch-strukturell unterscheidet sich Methadon deutlich von Morphin und Heroin. Die technische Synthese des racemischen Methadons ist recht einfach und geht aus von dem durch Kolbe-Nitrilsynthese leicht erhältlichen Diphenylacetonitril.[18]
Dabei wird das Diphenylacetonitril unter stark basischen Bedingungen (Natriumamid als Base) mit 1-Chlor-2-dimethylaminopropan zur Reaktion gebracht und dieses Produkt mit Ethylmagnesiumbromid in einer Grignard-Reaktion zum Methadon umgesetzt.[19]
Stereochemie Bearbeiten
Methadon ist chiral, es liegt daher in der Regel als 1:1-Gemisch (Racemat) von zwei spiegelbildlichen Molekülen (Enantiomeren) vor. Im Gegensatz zum linksdrehenden Levomethadon ist das rechtsdrehende Dextromethadon zwar ein potentes Antitussivum (Hustenblocker), besitzt aber nahezu keine analgetische Potenz. Daraus ergibt sich, dass Levomethadon (L-Polamidon) doppelt so stark analgetisch wirksam ist wie das rac-Methadon, und Levomethadon (L-Polamidon) demnach gegenüber rac-Methadon nur halb so hoch zu dosieren ist. In Deutschland sind rac-Methadon (Methaddict®[20]-Tabletten bzw. als Grundsubstanz) und Levomethadon zur Opioidsubstitution (z. B. bei Heroin) oder als starkes Schmerzmittel (Analgetikum) verschreibungsfähig (Nach Anlage III – BtMG BTM-Rezeptpflichtig) und ausschließlich über Apotheken beziehbar als Patient.
-
Levomethadon oder L-Methadon
-
Dextromethadon oder D-Methadon
Eine Trennung des racemischen Gemischs kann über diastereomere Salze mit L-(+)-Weinsäure erfolgen.[21][22]
Die reinen Enantiomere der freien Base schmelzen bei 100 °C. Das Racemat liegt als racemisches Gemisch mit einem eutektischen Schmelzpunkt von 77 °C vor. Enantiomerenreines Methadon-Hydrochlorid zeigt einen Schmelzpunkt bei 248 °C. Im Falle des 1:1-Gemisches der enantiomeren Hydrochloride wird eine racemische Verbindung mit einem Schmelzpunkt von 237 °C gebildet, die im Phasendiagramm eutektische Schmelzpunkte mit den Enantiomeren bei 233 °C bei Zusammensetzungen von 0.29/0,71 bzw. 0,71/0,29 zeigen.[5]
-
Phasendiagramm von Methadon Base
-
Phasendiagramm von Methadon-Hydrochlorid mit R – racemische Verbindung, E – Eutektikum
Analytik Bearbeiten
Methadon spricht als CH-azide Verbindung auf die Zimmermann/Janovski-Reaktion an. Dabei bildet es nach Zugabe von 1,3-Dinitrobenzol und Kaliumhydroxid in Methanol einen rot-violett gefärbten Meisenheimer-Komplex aus.
Die zuverlässige qualitative und quantitative Bestimmung von Methadon erfolgt nach angemessener Probenvorbereitung durch Kopplung der HPLC mit der Massenspektrometrie. Als Untersuchungsmaterial kommen in Frage Blut oder Speichel,[23] Haare,[24] Knochenmaterial,[25] Abwasserproben.[26] oder im Aerosol von Atemluftproben[27] Für verschiedene Untersuchungsgüter wurde auch der Einsatz der Gaschromatographie mit Massenspektrometrie-Kopplung beschrieben.[28][29]
Pharmakologie Bearbeiten
Methadon aktiviert den μ-Opioidrezeptor und entfaltet ab einer Dosis von 2,5 mg (bei erwachsenen Menschen) seine schmerzstillende, drei bis vier Stunden anhaltende Wirkung, die bezogen auf eine gleichmassige Einzeldosis das 1,5-Fache der von Morphin[30] beträgt. Methadon aktiviert weit weniger als Morphin das dopaminerge System im ventralen Tegmentum. Dies wird darauf zurückgeführt, dass Methadon im Gegensatz zu Morphin eine schwache Potenz an einem Rezeptorkomplex besitzt, der aus dem μ-Opioidrezeptor und dem Galaninrezeptor Typ 1 besteht. Aktivierung dieses Rezeptorheteromers ist mit Euphorisierung verbunden.[31]
Methadon hemmt dosisabhängig den HERG-Kanal, einen spannungsaktivierten, einwärtsgleichrichtenden Kaliumkanal in Herzmuskelzellen, wodurch es zu einer QT-Zeit-Verlängerung kommt (siehe Long-QT-Syndrom)[32].
Dextromethadon ist ein NMDA-Rezeptor-Antagonist. Dies erklärt dessen Wirkung bei neuropathischen Schmerzen.[8]
Methadon wird hauptsächlich über das Isoenzym CYP3A4 zu den inaktiven Metaboliten 2-Ethyliden-1,5-dimethyl-3,3-diphenylpyrrolidin (EDDP) und 2-Ethyl-5-methyl-3,3-diphenylpyralin (EMDP) abgebaut.[33] In geringerem Ausmaß spielen 2B6, 2C8, 2C18, 2C19 und 2D6 eine Rolle.[34][35] Die gleichzeitige Einnahme von Medikamenten, die diesen Abbauweg blockieren, führt zu einer Erhöhung der Plasmakonzentration von Methadon, ebenso wie die Einnahme von Medikamenten, die stark an Plasmaproteine gebunden werden, da Methadon zu 85–90 % an ebendiese Proteine gebunden wird. Umgekehrt kann Kokain die Plasmakonzentration von Methadon verringern.[36] Tabellarische Auflistungen der Interaktionen von Methadon mit anderen Medikamenten stehen zur Verfügung.[37]
Wirkungen Bearbeiten
Medizinische Wirkungen Bearbeiten
Methadon hat als Opioid dasselbe Wirkungs- und Nebenwirkungsprofil und somit im Wesentlichen dasselbe Gefahrenpotential wie andere Opioide (Ausnahme: Buprenorphin). Allerdings erzeugt es keinen Kick (jenes plötzliche intensive Wohlbefinden, das mit zur Entstehung einer Sucht führt).
Eingesetzt wird Methadon vor allem in unterschiedlichsten Abgabeprogrammen für Heroinabhängige. Diesbezüglich gilt eine Methadongabe als eine der wirksamsten Therapien überhaupt. Allerdings muss auch betont werden, dass ein Großteil der beabsichtigten Methadonwirkung auf der Tatsache beruht, dass es in besonderen, strukturierten Programmen angeboten wird.[16] Bei den meisten Teilnehmern führt eine tägliche Einmalgabe zur gewünschten Stabilisierung, wobei durch eine Cochrane-Studie zumindest zweifelsfrei belegt werden konnte, dass Patienten durch Methadon in Betreuung gehalten werden können und es zu weniger Heroin-Konsum kommt.[9] Zu beachten ist hier, dass (vom Patienten selbst als ausreichend bezeichnete) Dosierungen bis zu 40 mg durch handelsübliches Straßenheroin leicht „überwunden“ werden. Eine Opioidblockade-Wirkung kann erst ab Dosierungen von 60 mg erzielt werden: Das heißt, dass ein Beikonsum von handelsüblichen Opioiden wie Morphin, Heroin oder Hydromorphon keine narkotischen (und euphorisierenden) Effekte bewirkt.[38]
Einige Substituierte bauen Methadon schneller ab (sogenannte „fast metabolizer“), sodass es zum Ende eines 24-stündigen Dosierungsintervalls zu Entzugssymptomen kommen kann, und hier u. U. eine Abgabe in zwei Tagesdosen erfolgen muss.[16] Ist eine Abstinenz von Opioiden das Behandlungsziel, können bei langsamem Ausschleichen die Entzugssymptome erträglich gehalten werden. Auch der Heroinentzug selbst kann mit Methadon aufgefangen und zu Ende geführt werden (z. B. bei Krankenhaus- und Gefängnisaufenthalten). Ein langsames Ausschleichen von Methadon kann sich über mehrere Monate hinziehen und ab einer bestimmten Restmenge kann es zu unangenehmen Entzugserscheinungen kommen.
Untersuchte Wirkung in der Krebstherapie Bearbeiten
Die europäische Organisation zur Palliativversorgung („European Association for Palliative Care“, EPAC) empfiehlt Methadon als Schmerzmittel begleitend zur Krebstherapie, falls Patienten von Morphin nicht profitieren oder unter Nebenwirkungen leiden.[8]
Anfang der 1990er Jahre gab es erste präklinische Experimente über die Wirkung Methadons auf Lungenkrebs.[39] Eine mögliche verstärkende Wirkung auf Zytostatika als „Krebsmittel“ (wie beispielsweise Doxorubicin) ist Gegenstand von Untersuchungen, initiiert durch Claudia Friesen am Institut für Rechtsmedizin der Universität Ulm. Friesen hat bei In-vitro-Studien[40][41] postuliert, dass Methadon in verschiedenen soliden Tumoren und bei Leukämie einen Zelltod verursachen könne. Dabei soll eine vermutlich durch Methadon induzierte Aktivierung des µ-Opioidrezeptors (MOR) über inhibitorische Gi-Proteine zu einer Herunterregulierung von cAMP führen. Bei Leukämiezellen führe dies zur Apoptose, da Caspasen aktiviert werden.[42] Darüber hinaus soll Methadon den intrazellulären Calcium-Stoffwechsel stören, was eine morphologische und funktionelle Änderung der Mitochondrien verursacht.[43] Dennoch ist nicht genau bekannt, welcher antitumorale Mechanismus zugrunde liegt. So gibt es Hinweise darauf, dass Methadon bei Glioblastomzellen nicht über MOR zytotoxisch wirkt.[44] Bei den Zelllinien-Experimenten wurden zudem Methadon-Konzentrationen verwendet, die höher als die therapeutischen Spiegel waren. Weitere Experimente fanden an stark immundefizienten Nacktmäusen statt.[8] Dort wurde ein Effekt bei einer Methadondosis von 240 mg gezeigt. Die letale Tagesdosis bei nicht eingestellten Menschen beträgt 40 bis 60 mg, jedoch verstoffwechseln Mäuse Opioide schneller als Menschen.[45]
In einer retrospektiven Studie wurden aus einem Kollektiv von 938 Patienten mit Krebserkrankungen 76 identifiziert, die wegen Schmerzen von einem anderen Opioid auf Methadon umgestellt worden waren. Diese wurden mit 88 Patienten verglichen, die in ähnlicher Situation auf ein anderes Opioid umgestellt worden waren. In Hinblick auf das Gesamtüberleben zeigten sich keine Unterschiede.[46] Daten einer anderen Studie mit 52 Krebspatienten (Kopf-Halstumoren) ergaben ebenfalls keinen Hinweis auf einen Vorteil von Methadon hinsichtlich des Überlebens im Vergleich zu einem anderen Opioid (hier Fentanyl).[43]
Methadon wird in der Krebstherapie als klassisches Schmerzmittel angewandt, Anwendungsstudien haben bisher keinen antitumoralen Effekt bei Methadon (oder anderen Opioiden) belegt.[47][48] Die Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie sowie die Deutsche Gesellschaft für Neurologie[49] zweifeln an der Wirksamkeit von Methadon in der Krebstherapie und warnen vor unrealistischen Erwartungen,[50] die möglicherweise nach Veröffentlichung einer einzigen Studie von 2017 (mit 27 Krebspatienten mit Glioblastomen unterschiedlicher Stadien ohne Nennung einer Kontrollgruppe)[51] aufgekommen sein könnten.[52] Diese Studie analysierte zudem nur retrospektiv die Verträglichkeit der Methadongabe.[8] Der Sprecher im Vorstand der Neuroonkologischen Arbeitsgemeinschaft (NOA), Wolfgang Wick, hält die Datenbasis als Ansatz für eine mögliche Therapie für unzureichend.[53] Auch die Universität von Ulm, an dessen Institut für Rechtsmedizin die ersten wissenschaftlichen Erkenntnisse gewonnen wurden, distanziert sich ausdrücklich und hält den unkritischen Einsatz von Methadon außerhalb klinischer Studien für nicht gerechtfertigt.[54] Dem schlossen sich auch österreichische Gesellschaften wie das OeGHO[55] oder die ÖSG (Österreichische Schmerzgesellschaft)[56] an.
2017 verfasste das Ärztliche Zentrum für Qualität in der Medizin im Auftrag der Kassenärztlichen Bundesvereinigung und der Bundesärztekammer eine Patienteninformation zum Thema Methadon in der Krebstherapie.[57] Ebenfalls 2017 wurde die Finanzierung einer Studie bei der Deutschen Krebshilfe beantragt, um die Wirkung in der Krebstherapie zu überprüfen.[58] 2019 wurde eine klinische Prüfung bei Patienten mit metastasiertem Darmkrebs bewilligt, die Mitte 2023 gestartet ist („MEFOX-Studie“).[59][60][61] Bei Zellkulturexperimenten hat man dagegen bereits gezeigt, dass R-(−)-Methadon (Levomethadon) weder alleine noch in Kombination mit dem Chemotherapie-Medikament Temozolomid bei Glioblastomen wirksam ist.[62][63] Temozolomid zusammen mit einer Strahlentherapie gilt als therapeutischer Standard zur Erstlinienbehandlung von Glioblastomen.[44] Möglicher Grund für die fehlende Wirksamkeit ist das Fehlen von spezifischen Andockstellen (das aber in sonst keiner weiteren Studie gezeigt werden konnte), so dass Methadon keine Anti-Tumor-Wirkung bei den untersuchten Glioblastom-Zellkulturen entfalten könne. Eine Forschergruppe hat 2018 gezeigt, dass D-/L-Methadon mit oder ohne Temozolomid in Glioblastomzelllinien nur in hohen Dosen den Zelltod induziert – in Konzentrationen, die klinisch realisierbar sind, zeigte D-/L-Methadon in-vitro dagegen keinen Effekt.[64] Eine 2019 durchgeführte Studie bestätigte vorausgegangene Zellkulturexperimente: Bei aus Krebspatienten entnommenen Glioblastomzellen, die diesmal Rezeptoren aufweisen (mit gesunden Zellen zum Vergleich), entfaltet Methadon höchstens dann in Plasmakonzentrationen Wirkung, in denen es für Menschen tödlich wäre. Effektive Hirngewebskonzentrationen sind hingegen erreichbar.[65] Weitere Experimente raten ebenfalls von einer Therapie bei Glioblastomen von Methadon in Kombination mit Temozolomid wegen der fehlenden Wirkung in-vitro ab.[44]
Die Universität Ulm hält verschiedene Patente zur Anwendung von Methadon bzw. Opioiden bei Krebspatienten, in denen Friesen und andere als Erfinder genannt werden.[66]
Nebenwirkungen Bearbeiten
Eine Beurteilung der unerwünschten Wirkungen des Methadons ist von mehreren Voraussetzungen abhängig. Erstens kann ein Mensch mit einer seit mehreren Jahren bestehenden Opiatabhängigkeit bezüglich Wirkung und Nebenwirkungen eines Opiatersatzstoffes schwerlich einem Menschen mit geringer Drogenerfahrung gegenübergestellt werden. Zweitens können angegebene Nebenwirkungen des Medikaments als Symptome von Erkrankungen aufgefasst werden, die schon zur Zeit des Drogenkonsums bestanden oder durch den Drogenkonsum entstanden und zu diesem Zeitpunkt nicht entsprechend wahrgenommen oder berücksichtigt wurden. Drittens sind auch Besonderheiten der Drogenkultur mit ihren bestimmten Sichtweisen in Rechnung zu stellen.[67][68] Tatsächlich dürfte es so sein, dass viele unerwünschte Wirkungen als Folge einer zu Beginn der Substitutionsbehandlung ungeeigneten Medikamentendosis zu erklären sind.
So ist auch die gesuchte Euphorie aufgrund der Toleranzentwicklung trotz höherer Heroindosen zunehmend schwer zu erzielen. Dass Substituierte mit hohen Dosen an Methadon unter ausreichend langer Behandlung kaum mehr über unerwünschte Wirkungen – wie Schläfrigkeit und Benommenheit – klagen als Substituierte mit niedrigen Methadondosen (3,9 % gegenüber 4,3 %),[69] dürfte auf ebendiese Toleranzentwicklung zurückzuführen sein.
Nebenwirkungen können bei Methadondosen auftreten, die die vorbestehende Toleranz gegenüber Opioiden aufgrund des Vorkonsums überschreiten. Dies sind Müdigkeit, Schlafstörungen, Benommenheit, Übelkeit, Erbrechen, starkes Schwitzen, Ödeme (Flüssigkeitseinlagerung) in den Beinen, Harnverhaltung und Obstipation (Verstopfung). Sie verschwinden in der Regel mit der Toleranzentwicklung oder Reduktion der Dosis. Am längsten halten sich Schlaf- und sexuelle Störungen (bei einer Substitutionsdauer von drei Jahren noch in ca. 20 Prozent). Bis zu 50 Prozent der Substituierten klagen teilweise noch länger über verstärktes Schwitzen (Hyperhidrose).[38]
Spezifische Wirkungen Bearbeiten
Methaddict-Tabletten haben bei Einnahme während der Schwangerschaft eine Wirkung auf den Fötus. Deswegen wird empfohlen die Substitution mit Methadon vor der Geburt ausschleichend zu beenden. Wenn das Ausschleichen nicht möglich ist, muss der Entzug des Neugeborenen auf einer Kinderintensivstation durchgeführt werden. Es wurden Augenanomalien, neurologische Befunde mit Hörstörungen, geistigen und motorischen Entwicklungsverzögerungen und eine erhöhte Inzidenz von Otitis media beobachtet. Da Methadon über die Muttermilch ausgeschieden wird, muss im Einzelfall ein Arzt entscheiden, ob die Mutter ihr Kind stillen darf.[70]
Eine Verlängerung der QT-Zeit im EKG stellt einen Risikofaktor für das Auftreten von Herzrhythmusstörungen und hier besonders von potentiell lebensgefährlichen Torsade de pointes (TdP) dar. Eine Reihe von Faktoren wurde identifiziert, die die Wahrscheinlichkeit einer QT-Zeit-Verlängerung und nachfolgenden TdP erhöhen, nämlich weibliches Geschlecht, Hypokaliämie, verringerter Magnesium-Serumspiegel, bekannte Arzneimittelinteraktionen in der Vorgeschichte, bestehende Herzprobleme, ein unerkanntes angeborenes Long-QT-Syndrom (LQTS) und ein prädisponierender DNA-Polymorphismus. Zur Bedeutung dieser Faktoren für Methadonsubstituierte können bislang allerdings noch keine Angaben gemacht werden. Trotzdem müssen sie in der Substitutionstherapie berücksichtigt werden.[71] Etwa 2 % der Patienten, die Methadon erhalten, entwickeln eine verlängerte QT-Zeit, von diesen wieder rund 2 % Torsade de pointes. 2009 wurden in den USA Leitlinien für das QT-Zeit-Screening bei Methadonsubstitution veröffentlicht.[72] Verlängerungen der QT-Zeit und Torsade-de-pointes-Episoden waren ursprünglich auch der Grund für das Aussetzen der Vermarktung von LAAM.
Die QT-Zeit-Verlängerung wird hauptsächlich über Dextromethadon vermittelt, eine QT-Zeit-Verlängerung tritt daher auch nur bei der Substitution mit diesem Racemat auf. Eine durch das Racemat induzierte QT-Zeit-Verlängerung kann durch einen Wechsel der Substitution auf Levomethadon (L-Polamidon) rückgängig gemacht werden.[73] Für Dosen unter 100 mg pro Tag sind keine klinisch relevanten Veränderungen der QT-Zeit nachweisbar.[74]
Eine Methadongabe gilt als sicher, solange die Möglichkeit einer QT-Zeit-Verlängerung berücksichtigt, mittels EKG-Kontrollen vor der Therapie, einen Monat nach Therapiebeginn und dann in jährlichen Abständen überprüft wird, die Patienten informiert und entsprechende Konsequenzen aus den Ergebnissen gezogen werden. Somit empfehlen diese Richtlinien auch keinen Wechsel auf ein anderes Substitutionsmittel,[75][76] nachdem in den USA retardiertes Morphin, das keine QT-Zeit-Veränderung bewirkt, in Substitutionsprogrammen nicht zugelassen ist. In Österreich, Deutschland und der Schweiz ist ein Wechsel auf ebendieses retardierte Morphin möglich.
Intoxikation Bearbeiten
Zeichen einer Überdosierung von Opioiden sind bis zur Größe eines Stecknadelkopfes verengte Pupillen (Miosis), schwere Atemdepression und Bewusstseinsstörungen bis zum Koma (als sog. Opioidtrias), Blutdruckabfall mit Tachykardie, Hypothermie und abgeschwächte Reflexe bis zur Areflexie.[77] Bei Personen ohne Opioid-Toleranz können weniger als ein Milligramm pro Kilogramm Körpergewicht tödlich sein. Das heißt, dass die tödliche Dosis für ein Kleinkind weniger als 10 mg und für Erwachsene 40–50 mg betragen kann.[16] Bei einer Einstellung auf Methadon waren Todesfälle in den ersten zwei Wochen der Behandlung mit einem Dosisbereich von 25–100 mg verbunden, wobei die meisten bei Dosierungen von 40–60 mg auftraten. Wenn immer möglich sollten daher Patienten zur Zeit des ersten Wirkungsmaximums (drei bis vier Stunden nach der ersten Einnahme) auf Zeichen der Überdosierung (oder anhaltende Entzugssymptome) überprüft werden.[34] Zur Behandlung einer Überdosierung stehen antagonistisch wirkende Medikamente wie z. B. Naloxon oder Naltrexon zur Verfügung, wobei die Wirkdauer von ersterem wesentlich kürzer ist (ca. 1 Stunde) als die des Wirkstoffs Methadon bzw. Levomethadon (bis 48 Stunden atemdepressive Wirkung) und deshalb ggf. mehrfach nachdosiert werden muss.
Opioidabhängige mit regelmäßigem Konsum sind für eine Intoxikation weniger empfänglich als Gelegenheitskonsumenten oder Abhängige nach einem Opioidentzug.[77]
Anwendung Bearbeiten
Methadon ist in Tropfen- oder Tablettenform, in Österreich ausschließlich als Sirup, erhältlich. Es besitzt eine vergleichsweise hohe orale Bioverfügbarkeit von etwa 80 %.[78] Für die Einnahme wird es meist mit Zuckersirup, Saft oder Wasser verdünnt oder eingefärbt, um so bei einer Take-Home-Vergabe den missbräuchlichen intravenösen Konsum zu verhindern.[79][80] In Deutschland hat sich hauptsächlich die Verabreichung vor Ort von flüssigen Zubereitungen durchgesetzt.[79] Dies bietet den Vorteil, bei einer Abdosierung die Dosis langsam in sehr kleinen (bis hin zu tropfenweisen) Schritten verringern zu können, was Entzugserscheinungen zu vermeiden hilft. Überdies wird so vermieden, dass die Patienten ungeschluckte Tabletten anschließend wieder ausspucken, um sich diese später zu injizieren oder zu veräußern, wie es bei Subutex (Wirkstoff: Buprenorphin) oft geschieht. Methadontabletten können ohne vorherige Auflösung direkt eingenommen werden.
In Deutschland wird Levomethadon als hochpotentes Schmerzmittel zur Behandlung von starken akuten und chronischen Schmerzen eingesetzt. Das Medikament ist als Lösung (in einer Konzentration von 5 mg/ml[81]) zur oralen Anwendung und in Ampullen zur Injektion erhältlich. Eine retrospektive Kohortenstudie bei über 30.000 ausgewerteten Patientendaten hat ergeben, dass das Sterberisiko unter Methadon signifikant höher war als unter Morphin – selbst bei geringen Dosierungen.[82] Nach Ansicht der Autoren sollte daher Methadon nicht als erste Behandlungsoption für nicht-tumorbedingte Schmerzen eingesetzt werden.
Missbrauch und Weitergabe
Für Methadon existiert ein illegaler Markt, da einige Substituierte das Medikament nach der Abgabe durch die Apotheken weiterverkaufen.[83][84] Todesfälle in Zusammenhang mit Methadon erreichten in den USA seit der Jahrtausendwende vierstellige Fallzahlen. Bei Todesfällen mit verschreibungsfähigen opiathaltigen Schmerzmitteln wurde häufig festgestellt, dass die Verstorbenen sich diese ohne Rezept verschafft hatten und dass der Konsum in Kombination mit anderen, illegalen Substanzen erfolgte.[85]
In Österreich und einigen deutschen Substitutionsprogrammen muss der Patient auch deshalb sein Substitutionsmittel persönlich abholen. Ausnahmen werden in Deutschland mit der BTMVV §5 Absatz 7 und 9[86] und in Österreich mit § 23e der Rechtsvorschrift für die Suchtgiftverordnung geregelt.[87]
Die Weitergabe von Methadon ist untersagt, da es grundsätzlich den Bedingungen des Betäubungsmittelgesetzes unterliegt.
In Österreich ist eine Weitergabe des Substitutionsmittels Methadon nach dem Suchtmittelgesetz gerichtlich strafbar.
Zudem wird in den meisten Ländern regelmäßig untersucht, ob und welche Drogen noch konsumiert werden. Ein Ausschluss aus der Substitutionsbehandlung kann unter anderem erfolgen im Falle von
- Beigebrauch anderer Substanzen, die die Substitutionsbehandlung oder den Gesundheitszustand gefährden,
- Weitergabe oder intravenösen Anwendung des Substitutionsmittels,
- den widerrechtlichen Handel mit Suchtgiften oder suchtmittelhaltigen Arzneimitteln und
- der missbräuchlichen Verwendung von Rezepten.[88][87]
Handelsnamen Bearbeiten
Monopräparate: Heptadon (A), Levo-Methasan (A) Ketalgin (CH), Methaddict, Mephenon (FRA), (L-)Polamidon, L-Poladdict, L-Polaflux (D), Eptadone (D), Methaliq (D) sowie als Generikum (CH), L-Polamivet (Tiermedizin), Insistor (Tiermedizin)
Siehe auch Bearbeiten
Literatur Bearbeiten
- Hans V. Happel, Frank Männike: Über-Leben mit Methadon. Für eine alternative Drogenpolitik. Konkret Literatur, Hamburg 1992, ISBN 3-89458-116-6.
- U. Honegger, A. Seidenberg: Methadon, Heroin und andere Opioide: Medizinisches Manual für die ambulante opioidgestützte Behandlung. Huber, Bern u. a. 1998, ISBN 3-456-82908-6.
- R. Gerlach, H. Stöver: Vom Tabu zur Normalität – 20 Jahre Substitution in Deutschland. Lambertus, Freiburg i.Br. 2005, ISBN 3-7841-1605-1.
- Eberhard Klaschik: Schmerztherapie und Symptomkontrolle in der Palliativmedizin. In: Stein Husebø, Eberhard Klaschik (Hrsg.): Palliativmedizin. 5. Auflage. Springer, Heidelberg 2009, ISBN 3-642-01548-4, S. 207–313, hier: S. 234 und 248 f.
- Methadon in der Onkologie: „Strohhalmfunktion“ ohne Evidenz. In: Deutsches Ärzteblatt, 2017; 114(33-34), S. A-1530 / B-1298 / C-1269
Weblinks Bearbeiten
- Methadon. In: Erowid. (englisch)
- Methadon gegen Krebs? Arznei-Telegramm, 2. Juni 2017
- Hilft Methadon gegen Krebs? In: quarks.de. 29. Oktober 2019, abgerufen am 3. Januar 2019.
Einzelnachweise Bearbeiten
- ↑ a b Europäische Arzneibuch-Kommission (Hrsg.): Europäische Pharmakopöe 5. Ausgabe. Band 5.0 – 5.7, 2006.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Dextromethadon: CAS-Nummer: 5653-80-5, EG-Nummer: 637-187-9, ECHA-InfoCard: 100.164.915, PubChem: 643985, ChemSpider: 559067, DrugBank: DB15198, Wikidata: Q15634047.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Levomethadon: CAS-Nummer: 125-58-6, EG-Nummer: 603-081-6, ECHA-InfoCard: 100.120.592, PubChem: 22267, ChemSpider: 20904, DrugBank: DB13515, Wikidata: Q6535776.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Methadon Hydrochlorid: CAS-Nummer: 1095-90-5, EG-Nummer: 214-140-7, ECHA-InfoCard: 100.012.855, PubChem: 14184, ChemSpider: 13556, Wikidata: Q26840915.
- ↑ a b c d e M Kuhnert-Brandstätter, L. Friedl: Beitrag zur thermischen Analyse und zur Polymorphie optischer Antipoden: Pantolacton, Methadon und Usninsäure. In; Mikrochim. Acta 1979, Band 72, S. 97–110, doi:10.1007/BF01198052.
- ↑ a b c d Eintrag zu Methadone in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ a b Datenblatt (±)-Methadone hydrochloride bei Sigma-Aldrich, abgerufen am 10. April 2011 (PDF).
- ↑ a b c d e Friedemann Nauck et al.: Methadone as anticancer treatment: hype, hope, or hazard? In: Wiener Medizinische Wochenschrift. Band 168, Nr. 7-8, 1. Mai 2018, S. 159–167, doi:10.1007/s10354-018-0623-5.
- ↑ a b R. P. Mattick et al.: Methadone maintenance therapy versus no opioid replacement therapy for opioid dependence. (PDF; 369 kB) Cochrane Drugs and Alcohol Group, 2009.
- ↑ WHO Model List of Essential Medicines. (PDF; 442 kB) abgerufen am 20. September 2012.
- ↑ Foundation for a Drug-Free World: The Truth About Painkillers. In; Drug-Free World, S. 16. (eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ M. Bockmühl, G. Ehrhart: Verfahren zur Darstellung von basischen Estern. Deutsches Reichspatent Nr. 711069, Anmeldedatum: 11. September 1938, Veröffentlichung: 25. September 1941.
- ↑ P. O. Wolff: On pethidine and methadone derivatives. In: Bulletin of the World Health Organization, Band 2, Nummer 2, 1949, S. 193–204. PMID 15409516. PMC 2553950 (freier Volltext).
- ↑ C. C. Scott und K. K. Chen: The action of 1,1-diphenyl-1-(dimethylaminoisopropyl)-butanone-2, a potent analgesic agent. In: Federation proceedings, Band 5, Nummer 1, 1946, S. 201. PMID 20983210.
- ↑ E. M. Stoya: M wie Methadon. ( vom 9. September 2012 im Webarchiv archive.today) In: Die PTA in der Apotheke, 11, 2011, S. 20.
- ↑ a b c d Nicholas Seivewright, assisted by Mark Parry: Community Treatment of Drug Misuse: More Than Methadone. Cambridge University Press, 2009.
- ↑ A. Ulmer, R. Ullmann: Nachruf Gorm Grimm. ( vom 24. November 2015 im Internet Archive) (PDF; 292 kB) In: Suchttherapie, 9, 2008, S. 185–186. doi:10.1055/s-0028-1102925.
- ↑ Eberhard Breitmaier: Alkaloide. Teubner-Verlag, 1997, S. 158.
- ↑ Patent US2443246: Preparation of certain diarylacetonitriles. Angemeldet am 9. Dezember 1946, veröffentlicht am 15. Juni 1948, Erfinder: August H. Homeyer, Janet S. Splitter (Mallinckrodt).
- ↑ Methaddict® ist der patentiert Handelsname von Hexal
- ↑ Patent US2644010: Salts of D-amidone with an optically active acid and process for resolving DL-amidone. Veröffentlicht am 30. Juni 1953, Erfinder: Eugene E. Howe, Max Tishler (MSD).
- ↑ Patent US2983757: Resolution of DL-methadone. Veröffentlicht am 9. Mai 1961, Erfinder: Harold E. Zaugg (Abbott).
- ↑ Strand MC, Ramaekers JG, Gjerde H, Mørland J, Vindenes V: Pharmacokinetics of Single Doses of Methadone and Buprenorphine in Blood and Oral Fluid in Healthy Volunteers and Correlation With Effects on Psychomotor and Cognitive Functions., J Clin Psychopharmacol. 2019 Sep/Oct;39(5), S. 489–493, PMID 31305338
- ↑ R. Kronstrand, M. Forsman, M. Roman: Quantitative analysis of drugs in hair by UHPLC high resolution mass spectrometry., Forensic Sci Int. 2018 Feb;283, S. 9–15, PMID 29241093
- ↑ M. Vandenbosch, T. Somers, E. Cuypers: Distribution of Methadone and Metabolites in Skeletal Tissue., J Anal Toxicol. 2018 Jul 1;42(6), S. 400–408, PMID 29490025
- ↑ R. Bade, JM. White, C. Gerber: Qualitative and quantitative temporal analysis of licit and illicit drugs in wastewater in Australia using liquid chromatography coupled to mass spectrometry., Anal Bioanal Chem. 2018 Jan;410(2), S. 529–542, PMID 29214532
- ↑ S. Ullah, S. Sandqvist, O. Beck: A liquid chromatography and tandem mass spectrometry method to determine 28 non-volatile drugs of abuse in exhaled breath., J Pharm Biomed Anal. 2018 Jan 30;148, S. 251–258, PMID 29059614
- ↑ A. Ribeiro, M. Prata, C. Vaz, T. Rosado, J. Restolho, M. Barroso, Araújo Gallardo. ARTSE: Determination of methadone and EDDP in oral fluid using the dried saliva spots sampling approach and gas chromatography-tandem mass spectrometry., Anal Bioanal Chem. 2019 Apr;411(10), S. 2177–2187, PMID 30824966
- ↑ YC. Hsu, BG. Chen, SC. Yang, YS. Wang, SP. Huang, MH. Huang, TJ. Chen, HC. Liu, DL. Lin, RH. Liu, AW. Jones: Methadone concentrations in blood, plasma, and oral fluid determined by isotope-dilution gas chromatography-mass spectrometry., Anal Bioanal Chem. 2013 May;405(12), S. 3921–3928, PMID 23090648
- ↑ Eberhard Klaschik: Schmerztherapie und Symptomkontrolle in der Palliativmedizin. 2009, S. 234.
- ↑ NS. Cai, C. Quiroz, J. Bonaventura et al.: Opioid-galanin receptor heteromers mediate the dopaminergic effects of opioids. In: J. Clin. Invest. Band 129, Heft 7, 2019, S. 2730–2744, doi:10.1172/JCI126912, PMID 30913037, PMC 6597217 (freier Volltext) – (jci.org).
- ↑ C B Eap, S Crettol, J-S Rougier, J Schläpfer, L Sintra Grilo: Stereoselective Block of hERG Channel by (S)-Methadone and QT Interval Prolongation in CYP2B6 Slow Metabolizers. In: Clinical Pharmacology & Therapeutics. Band 81, Nr. 5, 28. Februar 2007, S. 719–728, doi:10.1038/sj.clpt.6100120.
- ↑ Yutaka Oda, Evan D. Kharasch: Metabolism of Methadone andlevo-α-Acetylmethadol (LAAM) by Human Intestinal Cytochrome P450 3A4 (CYP3A4): Potential Contribution of Intestinal Metabolism to Presystemic Clearance and Bioactivation. In: J Pharmacol Exp Ther, 298(3), Sep 2001, S. 1021–1032. PMID 11504799.
- ↑ a b Richard P. Mattick et al.: Pharmacotherapies for the Treatment of Opioid Dependence: Efficacy, Cost-Effectiveness and Implementation Guidelines. Informa Healthcare, 2009, ISBN 978-1-84184-400-8.
- ↑ B. Stewart et al.: When “Enough” is not Enough: New Perspectives on Optimal Methadone Maintenance Dose. ( vom 15. April 2011 im Internet Archive) (PDF; 95 kB) In: Mount Sinai Journal of Medicine, Volume 67, Number 5 & 6, Oct–Nov 2000, S. 404–411.
- ↑ E. F. McCance-Katz, P. Jatlow, P. M. Rainey: Effect of cocaine use on methadone pharmacokinetics in humans. In: Am J Addict., 19(1), Jan–Feb 2010, S. 47–52. PMID 20132121.
- ↑ Elinore F. McCance-Katz: Methadone-Drug Interactions (Medications, illicit drugs, & other substances). ( vom 19. Oktober 2013 im Internet Archive) (PDF; 675 kB).
- ↑ a b Richard A. Rettig, Adam Yarmolinsky, Institute of Medicine (U.S.). Committee on Federal Regulation of Methadone Treatment: Federal regulation of methadone treatment. 1995.
- ↑ Tatjana Vatter et al.: Against Repurposing Methadone for Glioblastoma Therapy. In: Biomolecules. Band 10, Nr. 6, 17. Juni 2020, S. E917, doi:10.3390/biom10060917, PMID 32560384, PMC 7356722 (freier Volltext).
- ↑ C. Friesen: Opioid receptor activation triggering downregulation of cAMP improves effectiveness of anti-cancer drugs in treatment of glioblastoma. In: Cell Cycle, 2014, 13(10), S. 1560–1570.
- ↑ C. Friesen et al.: Cell death sensitization of leukemia cells by opioid receptor activation. In: Oncotarget, 2013, 4(5), S. 677–690.
- ↑ S. Wirz et al.: Einsatz von Methadon zur Unterstützung der onkologischen Therapie? In: Der Schmerz. Band 31, Nr. 1, 1. Februar 2017, S. 2–4, doi:10.1007/s00482-016-0183-9.
- ↑ a b Marieke H. J. van den Beuken-van Everdingen, Sander M. J. van Kuijk und Elbert A. Joosten: Response to the Article "Overall Survival among Cancer Patients Undergoing Opioid Rotation to Methadone Compared to Other Opioids". In: Journal of Palliative Medicine. Band 20, Nr. 11, November 2017, S. 1184–1185, doi:10.1089/jpm.2017.0301, PMID 28731784.
- ↑ a b c Bodo Haas et al.: Methadone-mediated sensitization of glioblastoma cells is drug and cell line dependent. In: Journal of Cancer Research and Clinical Oncology. Band 147, Nr. 3, 1. März 2021, S. 779–792, doi:10.1007/s00432-020-03485-3, PMID 33315125, PMC 7872955 (freier Volltext).
- ↑ Hilft Methadon gegen Krebs? In: quarks. 29. Oktober 2019, abgerufen am 21. Januar 2020.
- ↑ Akhila Reddy et al.: Overall Survival among Cancer Patients Undergoing Opioid Rotation to Methadone Compared to Other Opioids. In: Journal of Palliative Medicine. Band 20, Nr. 6, Juni 2017, S. 656–661, doi:10.1089/jpm.2016.0316, PMID 27997283.
- ↑ Philip J. Wiffen et al.: Opioids for cancer-related pain in children and adolescents. In: The Cochrane Database of Systematic Reviews. Band 7, 19. Juli 2017, S. CD012564, doi:10.1002/14651858.CD012564.pub2, PMID 28722116.
- ↑ S. Mercadante, A. Casuccio und L. Calderone: Rapid switching from morphine to methadone in cancer patients with poor response to morphine. In: Journal of Clinical Oncology: Official Journal of the American Society of Clinical Oncology. Band 17, Nr. 10, Oktober 1999, S. 3307–3312, doi:10.1200/JCO.1999.17.10.3307, PMID 10506634.
- ↑ Nina Buschek: Hirntumor: Methadon verstärkt nicht die Wirksamkeit der Chemotherapie. Archiviert vom am 23. Juni 2018; abgerufen am 23. Juni 2018. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Methadon bei Krebspatienten: Zweifel an Wirksamkeit und Sicherheit. DGHO, abgerufen am 17. August 2017.
- ↑ J. Onken et al.: Safety and Tolerance of D,L-Methadone in Combination with Chemotherapy in Patients with Glioma. In: Anticancer Research, Band 37, Nummer 3, 03 2017, S. 1227–1235, doi:10.21873/anticanres.11438, PMID 28314286.
- ↑ plusminus 16. August 2017 daserste.de ( vom 20. August 2017 im Internet Archive)
- ↑ Felix Hütten: Methadon - Wundermittel gegen Krebs? In: sueddeutsche.de. 24. Juli 2017 (sueddeutsche.de [abgerufen am 23. Juni 2018]).
- ↑ Stellungnahme zur Tumortherapie mit Methadon. (uniklinik-ulm.de [abgerufen am 23. Juni 2018]).
- ↑ Stellungnahme - Methadon bei Krebspatienten - News - oegho.at. Abgerufen am 4. Januar 2019.
- ↑ Methadon bei Tumorpatienten Stellungnahme der Österreichischen Schmerzgesellschaft (ÖSG). Österreichischen Schmerzgesellschaft, 10. Juli 2017, archiviert vom am 4. Januar 2019; abgerufen am 4. Januar 2019. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Methadon. Bislang kein Nutzen belegt: Methadon in der Krebsbehandlung. Patienten-Information.de, abgerufen am 29. Januar 2018.
- ↑ Deutsche Krebshilfe will 5 neue Zentren mit 50 Millionen Euro fördern. In: Deutsches Ärzteblatt. 5. Juli 2017, abgerufen am 29. Januar 2018.
- ↑ Thomas Burmeister: Hilft Methadon bei Krebs? Ärzte Zeitung, 28. Oktober 2019, abgerufen am 8. Januar 2020.
- ↑ Melanie Güthle et al.: Eine Phase I/II Studie zur Therapie mit D,L-Methadon und mFOLFOX6 in der Behandlung des fortgeschrittenen kolorektalen Karzinoms: Die MEFOX Studie (AIO-KRK-0119). In: Zeitschrift für Gastroenterologie. Band 59. Georg Thieme Verlag KG, August 2021, S. e185, doi:10.1055/s-0041-1733553.
- ↑ Clemens Haug: Methadon in der Krebstherapie: Klinische Studie ist angelaufen. In: mdr.de. 12. Mai 2023, abgerufen am 21. Juni 2023.
- ↑ Nina Buschek: Hirntumor: Methadon verstärkt nicht die Wirksamkeit der Chemotherapie. Archiviert vom am 23. Juni 2018; abgerufen am 30. September 2018. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Bettina Jung: Methadon im Zellversuch beim Glioblastom unwirksam. In: DAZ.online. 1. März 2018 (deutsche-apotheker-zeitung.de [abgerufen am 2. Oktober 2018]).
- ↑ Konstantin Brawanski et al.: Efficacy of D,L-methadone in the treatment of glioblastoma in vitro. In: CNS oncology. Band 7, Nr. 3, 1. Juli 2018, S. CNS18, doi:10.2217/cns-2018-0006, PMID 29916277, PMC 6200059 (freier Volltext).
- ↑ Vera Zylka-Menhorn: Glioblastome: Leipziger Studie – Methadon bei Therapie von Hirntumoren unwirksam. Deutsches Ärzteblatt, 19. April 2019, abgerufen am 27. Mai 2019.
- ↑ METHADON-HYPE BEI KREBS … Emotionen ersetzen Wirksamkeitsbelege. Arznei-Telegramm, 15. September 2017, abgerufen am 11. März 2020.
- ↑ Douglas Goldsmith et al. Methadone Folklore: Beliefs about Side Effects and Their Impact on Treatment. In: Human Organization, 43, 1984, S. 330, doi:10.17730/humo.43.4.64m061v484th3871.
- ↑ Dana E. Hunt, Douglas S. Lipton, Douglas S. Goldsmith, David L. Strug, Barry Spunt: Substance Use & Misuse. Band 20, No. 11–12, 1985, S. 1751–1771, doi:10.3109/10826088509047261
- ↑ Eric C. Strain et al.: Moderate- vs High-Dose Methadone in the Treatment of Opioid Dependence – A Randomized Trial. In: JAMA, 281, 1999, S. 1000–1005.
- ↑ Ruthard Stachowske, Website der Evangelischen Hochschule Dresden, abgerufen am 22. März 2020.
- ↑ J. Stringer, C. Welsh und A. Tommasello: Methadone-associated Q-T interval prolongation and torsades de pointes. In: Am J Health Syst Pharm. 66(9), 1. Mai 2009, S. 825–833. PMID 19386945
- ↑ QT-Zeit-Screening bei Methadon ( vom 15. August 2009 im Internet Archive) – US-Leitlinie 2009.
- ↑ Nicolas Ansermot et al.: Substitution of (R,S)-Methadone by (R)-Methadone – Impact on QTc Interval Clinical Guidelines. In: Archives of Internal Medicine., Band 170 No. 6, 22. Mar 2010, S. 529–536.
- ↑ Stallvik et al.: Corrected QT interval during treatment with methadone and buprenorphine--relation to doses and serum concentrations. Drug And Alcohol Dependence, PMID 23084592
- ↑ Mori J. Krantz et al.: Clinical Guidelines – QTc Interval Screening in Methadone Treatment. In: Annals of Internal Medicine, vol. 150 no. 6, 17. Mar 2009, S. 387–395.
- ↑ Mori J. Krantz et al.: Concerns About Consensus Guidelines for QTc Interval Screening in Methadone Treatment. In: Ann Intern Med., 151, 2009, S. 218–219. PMID 19652193
- ↑ a b E. Freye: Opioide in der Medizin. 8. Auflage. Springer, 2010, ISBN 978-3-540-88796-6.
- ↑ Michael Krausz, Christian Haasen und Dieter Naber: Pharmakotherapie der Sucht. Karger Medical and Scientific Publishers, 2003, ISBN 3-8055-7482-7.
- ↑ a b Felix Tretter und Max Braun: Suchtmedizin kompakt: Suchtkrankheiten in Klinik und Praxis; mit 51 Tabellen. Schattauer Verlag, 2008, ISBN 978-3-7945-2611-6, S. 213.
- ↑ Karlheinz Keppler, Heino Stöver: Gefängnismedizin: Medizinische Versorgung unter Haftbedingungen. Georg Thieme Verlag, 2009, ISBN 978-3-13-157001-7.
- ↑ Eberhard Klaschik: Schmerztherapie und Symptomkontrolle in der Palliativmedizin. 2004, S. 234 (Levo-Methadon).
- ↑ Wayne A. Ray et al.: Out-of-hospital mortality among patients receiving methadone for noncancer pain. In: JAMA internal medicine. Band 175, Nr. 3, März 2015, S. 420–427, doi:10.1001/jamainternmed.2014.6294, PMID 25599329, PMC 4346542 (freier Volltext).
- ↑ W. R. Davis, B. D. Johnson: Prescription opioid use, misuse, and diversion among street drug users in New York City. In: Drug and alcohol dependence, Band 92, Nummer 1–3, Januar 2008, S. 267–276, doi:10.1016/j.drugalcdep.2007.08.008. PMID 17913395. PMC 2317747 (freier Volltext).
- ↑ Metha-Spritz-Umfrage (PDF; 256 kB) akzept.org
- ↑ National Prescription Drug Threat Assessment. (PDF; 3,1 MB) National Drug Intelligence Center, USA, April 2009, S. 23–24.
- ↑ § 5 BtMVV - Einzelnorm. Abgerufen am 9. März 2021.
- ↑ a b Rechtsvorschrift für Suchtgiftverordnung in Österreich. Fassung vom 16. Dezember 2009 (mit Behandlungsvertrag).
- ↑ Budesärztekammer: Richtlinie der Bundesärztekammer zur Durchführung der substitutionsgestützten Behandlung Opioidabhängiger. (PDF) Bundesärztekammer, 28. April 2017, abgerufen am 10. März 2021.