Tranexamsäure
Tranexamsäure (AMCHA oder TXA) ist ein Arzneistoff, der in der Medizin zur Hemmung des Fibrinolysesystems verwendet wird (Antifibrinolytikum, Fibrinolysehemmer). Der Wirkungsmechanismus beruht auf einer Komplexbildung mit Plasminogen, wodurch dessen Bindung an die Fibrinoberfläche gehemmt wird. Damit resultiert letztlich eine Hemmung der Gerinnselauflösung (Fibrinolyse).
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
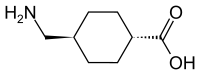
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Tranexamsäure[1] | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C8H15NO2 | |||||||||||||||||||||
| Kurzbeschreibung |
beigefarbener Feststoff[3] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse |
Fibrinolyse-Hemmer | |||||||||||||||||||||
| Wirkmechanismus |
Lysin-Analog | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 157,21 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
| Pharmakologische Informationen | |||
|---|---|---|---|
| Verabreichungsart | peroral (p.o.); intravenös (i.v.); lokal | ||
| Bioverfügbarkeit | 30–50 % nach peroraler Gabe, unbeeinträchtigt durch gleichzeitige Nahrungsaufnahme. Plazentagängig 100 %. Plasmaproteinbindung 3 % (fast ausschließlich an Plasmin). Muttermilchgängig 1 %. | ||
| Metabolismus | geringfügig in der Leber; terminale Halbwertszeit 2 Stunden, Verteilungsvolumen 9–12 Liter | ||
| Wechselwirkungen | Faktor IX | erhöhtes Thromboserisiko | |
| Ausscheidung | Urin | 95 % als unveränderte Substanz | |
| Klinische Informationen | |||
| Nebenwirkungen | Sehstörungen, Übelkeit, Erbrechen, Durchfall. Blutdruckabfall (bei schneller i.v. Gabe). | ||
| Kontraindikation(en) | Niereninsuffizienz, Harnwegsblutung, bestehende Thrombosen. | ||
| Zulassungsstatus | |||
| Deutschland | USA | UK | |
| Erstzulassung oder Markteinführung | 1967 (Anvitoff) | 1986 (Cyklokapron) | 1978 (Cyklokapron) |
| Verschreibungspflicht | ja | ja | ja |
Eigenschaften
BearbeitenTranexamsäure ist ein synthetischer Stoff, der der Aminosäure Lysin ähnelt. Er zählt wie ε-Aminocapronsäure und p-Aminomethylbenzoesäure zur Gruppe der sogenannten ε-Aminocarbonsäuren.
Tranexamsäure ist leicht löslich in Wasser und Eisessig, sowie praktisch unlöslich in Aceton und in Ethanol (96 %).[5] Tranexamsäure in pharmazeutischer Qualität ist ein weißes bis fast weißes kristallines Pulver.[5]
Wirkungsmechanismus
BearbeitenTranexamsäure blockiert die Bildung von Plasmin durch Hemmung der proteolytischen Aktivität der Plasminogenaktivatoren. Dadurch wird Plasmin in seiner Fähigkeit Fibrin zu lysieren behindert. Bei niedriger Dosis wirkt Tranexamsäure als kompetitiver Hemmer des Plasmins, bei hoher Dosierung als nicht-kompetitiver Hemmer. Alle ε-Aminocarbonsäuren wirken analog.
Pharmakokinetik
BearbeitenAufnahme und Bioverfügbarkeit
BearbeitenTranexamsäure ist nach peroraler Gabe zu 30–50 % bioverfügbar.[6] Das Verteilungsvolumen beträgt 9–12 L.[7] Die Halbwertszeit ist 2 Stunden.[6]
Verstoffwechselung
BearbeitenTranexamsäure wird nur sehr geringfügig in der Leber verstoffwechselt. Als Stoffwechselprodukte haben sich eine Dicarboxylsäure (1 % der verabreichten Dosis) und die acetylierte Form von Tranexamsäure (0,1 % der verabreichten Dosis) im Urin vorfinden lassen.[8]
Ausscheidung
BearbeitenDie Ausscheidung erfolgt zu 95 % über die Nieren und Harnwege (renale Elimination). Auf Grund der fast ausschließlich renalen Eliminierung des Stoffs muss die Dosis bei Niereninsuffizienz vor allem bei längerer Anwendung reduziert werden, damit keine Akkumulation von Tranexamsäure im Plasma erfolgt. In Abhängigkeit vom Kreatinin im Serum wird die Anzahl der Einzeldosen pro Tag vermindert.[9][10]
Wechselwirkungen
BearbeitenBei gemeinschaftlicher Verabreichung von Tranexamsäure und Faktor IX bei Hämophilie wird kein erhöhtes Thromboserisiko beobachtet.[11]
Anwendungsgebiete
Bearbeiten- Zur Verhinderung oder Linderung von Blutungen bei Zahnextraktion oder Zahnfleischblutungen bei Hämophilie.[12]
- Generalisierte und/oder lokale Hyperfibrinolyse (verstärkte Fibrinolyse). Minderung der Hyperfibrinolyse, entstanden entweder durch Überschuss an Plasmin (Hyperplasminämie) oder als Folge einer thrombolytischen Behandlung mit beispielsweise Streptokinase. Eine erhöhte lokale Fibrinolyse kann bei Prostataoperationen und Operationen an den Harnwegen, bei rezidivierenden Blutungen des Gastrointestinaltraktes, bei Colitis ulcerosa, bei essentieller oder durch ein Intrauterinpessar (IUP) induzierter Hypermenorrhoe (vermehrter Monatsblutung), bei Nasenbluten und nach Zahnextraktion bei Patienten mit Gerinnungsstörungen (Koagulopathien) auftreten. Ebenso wird Tranexamsäure bei Operationen mit extrakorporalem Kreislauf (Herz-Lungen-Maschine) verwendet und auch beim akuten Schädel-Hirn-Trauma[13] eingesetzt.
- Tranexamsäure findet als Antidot (Gegenmittel) bei der Blockierung von Fibrinolytika wie Streptokinase eine weitere Anwendung. Alternativ gab man hier auch den Proteinaseinhibitor (Antiplasmin) Aprotinin, der wegen seiner thrombogenen Wirkung 2007 vom Markt genommen wurde.[12]
- Hereditäres Angioödem (HAE).[14]
Nebenwirkungen
Bearbeiten- Allergische Reaktionen kommen sowohl systemisch (am ganzen Körper) als auch in Form von Hautausschlägen vor.
- Tranexamsäure kann insbesondere bei Patienten mit angeborener oder erworbener Neigung zu Thrombosen (Thrombophilie) zu einer Bildung oder Vermehrung von Thrombosen führen. Thrombosen können nachfolgend zu Embolien führen (Lungenembolie, Schlaganfall). Eine Meta-Analyse von 216 Studien zur Häufigkeit thrombotischer Komplikationen nach der intravenösen Gabe von Tranexamsäure fand kein erhöhtes Risiko im Vergleich zu Placebo oder keinem Eingriff.[15] Die Meta-Analyse legt nahe, dass intravenös verabreichte TXA auch unabhängig von der Dosierung das Risiko thromboembolischer Ereignisse nicht erhöht. Allerdings kritisieren mehrere Kommentatoren die Heterogenität der Studien.[16]
- Vorhofflimmern mit erhöhtem Schlaganfallrisiko.
- Tranexamsäure kann bei Menschen Sehstörungen auslösen. Im Tierexperiment wurden Schädigungen der Netzhaut beschrieben.
Gegenanzeigen
Bearbeiten- Stillzeit. Tranexamsäure geht in die Muttermilch über (in sehr geringen Konzentrationen von ca. 1 % der Plasmakonzentration).
- Blutungen im Harntrakt. Es können durch Anwendung von Tranexamsäure Verstopfungen der Harnleiter mit nachfolgendem Urinaufstau entstehen.
- Thrombosen. Thrombosen (vorbestehend) werden bei Gabe von Tranexamsäure gefördert.
- Sepsis und DIC (disseminierte intravasale Gerinnung).
Handelspräparate
Bearbeiten- Cyklokapron Filmtabletten 500 mg / Injektions-Infusionslösung 100 mg/ml (D, A, USA); Lysteda Tabletten 650 mg (USA)
- Kombinationspräparat mit humanem Fibrin und Thrombin (Fibrinkleber): Quixil (D; a.H.)
Einzelnachweise
Bearbeiten- ↑ INN Recommended List 7, World Health Organisation (WHO), 9. Dezember 1967.
- ↑ Eintrag zu TRANEXAMIC ACID in der CosIng-Datenbank der EU-Kommission, abgerufen am 12. Dezember 2021.
- ↑ a b c d Datenblatt trans-4-(Aminomethyl)cyclohexanecarboxylic acid, 97% bei Sigma-Aldrich, abgerufen am 24. April 2011 (PDF).
- ↑ a b c Eintrag zu Tranexamsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 28. Dezember 2014.
- ↑ a b Monographie „Tranexamic acid“, European Pharmacopoeia 10th Edition, 1st Supplement (Ph. Eur. 10.1), EDQM Council of Europe, 2019.
- ↑ a b Andrew Wilcock, Claudia Bausewein, Constanze Rémi, Paul Howard, Sarah Charlesworth: Arzneimitteltherapie in der Palliativmedizin. Elsevier Health Sciences, 2021, ISBN 978-3-437-06366-4, S. 231 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Bundesinstitut für Arzneimittel und Medizinprodukte: Tranexamsäure antifibrinolytics art 31(TXA)_annexI_III_de, abgerufen am 11. Dezember 2023
- ↑ FDA: LYSTEDA® (tranexamic acid) tablets, for oral use Initial U.S. Approval: 1986, abgerufen am 11. Dezember 2023
- ↑ Å. Pilbrant, M. Schannong, J. Vessman: Pharmacokinetics and bioavailability of tranexamic acid. In: European Journal of Clinical Pharmacology. Band 20, Nr. 1, 1981, S. 65–72, doi:10.1007/BF00554669.
- ↑ L. Andersson, O. Eriksson, P.-O. Hedlund, H. Kjellman, B. Lindqvist: Special considerations with regard to the dosage of tranexamic acid in patients with chronic renal diseases. In: Urological Research. Band 6, Nr. 2, 1978, S. 83–88, doi:10.1007/BF00255578.
- ↑ Benjamin Djulbegovic, Margaret M. Hannan, Garrett E. Bergman: Concomitant Treatment with Factor IX Concentrates and Antif ibrinolytics in Hemophilia B. In: Acta Haematologica. Band 94, Suppl. 1, 2009, S. 43–48, doi:10.1159/000204027.
- ↑ a b Isabell Pekrul, Thomas Schachtner, Bernhard Zwißler, Patrick Möhnle: Tranexamsäure zur Blutungsprophylaxe bei Trauma und orthopädischen Eingriffen – Standard oder individualisierte Anwendung? In: Der Anaesthesist. Band 70, Nr. 6, 2021, S. 515–521, doi:10.1007/s00101-021-00928-5, PMID 33620508.
- ↑ Nicola Siegmund-Schultze: Akutes Schädel-Hirn-Trauma. Tranexamsäure, früh infundiert, verringert verletzungsbedingte Sterblichkeit. In: Deutsches Ärzteblatt. Band 116, Heft 51 f., 23. Dezember 2019, S. B 1974 f.
- ↑ Andreas Recke: Fortschritte in Diagnostik und Therapie des hereditären Angioödems. In: hautnah dermatologie. Band 38, Nr. 3, 2022, S. 56–66, doi:10.1007/s15012-022-6896-9, PMC 9124601 (freier Volltext).
- ↑ Isabel Taeuber et al.: Association of Intravenous Tranexamic Acid With Thromboembolic Events and Mortality. In: JAMA Surg. April 2021, doi:10.1001/jamasurg.2021.0884.
- ↑ John B. Holcomb et al.: Tranexamic Acid and Safety in the Right Patient. In: JAMA Surg. April 2021, doi:10.1001/jamasurg.2021.0929.