Praseodym(III)-nitrat
chemische Verbindung
Praseodym(III)-nitrat (Pr(NO3)3) ist ein Salz des Seltenerd-Metalls Praseodym mit Salpetersäure.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
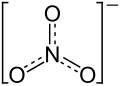
| ||||||||||
| Allgemeines | ||||||||||
| Name | Praseodym(III)-nitrat | |||||||||
| Andere Namen |
| |||||||||
| Summenformel |
| |||||||||
| Kurzbeschreibung |
hellgrüner Feststoff (Hexahydrat)[2] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | ||||||||||
| Aggregatzustand |
fest | |||||||||
| Schmelzpunkt |
≈56 °C[3] | |||||||||
| Löslichkeit |
löslich in Wasser, 80 g·l−1 (22 °C) (Hexahydrat)[3] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Darstellung
BearbeitenKristalle des Hexahydrats können aus Lösungen von Pr6O11 in verdünnter Salpetersäure gezüchtet werden.[3]
Eigenschaften
BearbeitenPraseodym(III)-nitrat bildet als Hexahydrat grüne Kristalle. Es ist unter Normalbedingungen stabil. Bei erhöhten Temperaturen verliert es allmählich das Kristallwasser, oberhalb von 253 °C wird die wasserfreie Form erhalten. Ab ca. 310 °C findet Zersetzung zu Praseodymoxidnitrat (PrONO3) und Stickoxiden statt.[1]
Einzelnachweise
Bearbeiten- ↑ a b F. J. Rey, J. Martín-Gil, A. Gonzáles, F. J. Martín-Gil: Kinetic analysis of thermal decomposition of praseodymium(III) nitrate hexahydrate. In: Journal of thermal analysis. Band 35, Nr. 3, 1. Mai 1989, S. 805–813, doi:10.1007/BF02057236.
- ↑ a b c Datenblatt Praseodym(III)-nitrat Hexahydrat bei Sigma-Aldrich, abgerufen am 10. November 2021 (PDF).
- ↑ a b c J. Newton Friend: 346. The nitrates of neodymium and praseodymium, and their solubilities in water. In: Journal of the Chemical Society (Resumed). 1935, S. 1430, doi:10.1039/jr9350001430.


