Histidinol
chemische Verbindung
Histidinol ist eine chemische Verbindung aus der Gruppe der chiralen 1,2-Aminoalkohole. Histidinol ist eine Vorstufe der Aminosäure Histidin, und kommt natürlich, wie auch Histidin, enantiomerenrein in der (S)-Konfiguration vor. Das Enantiomer (R)-Histidinol und das racemische (RS)-Histidinol besitzen nur geringe Bedeutung.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
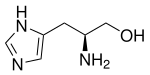
| |||||||||||||||||||
| (S)-Histidinol | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Histidinol | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H111N3O | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 141,17 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest (Dihydrochlorid) | ||||||||||||||||||
| Schmelzpunkt |
198–201 °C (Dihydrochlorid)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Gewinnung und Darstellung
Bearbeiten(S)-Histidinol kann durch Reduktion von Benzoyl-L-histidinmethylester mit Lithiumaluminiumhydrid und anschließender Hydrolyse als Dihydrochlorid hergestellt werden.[2]
Vorkommen
Bearbeiten(S)-Histidinol kommt als Zwischenprodukt bei der Biosynthese von Histidin vor. Dabei wird es zunächst mit NAD zu Histidinal und anschließend erneut mit NAD zu Histidin oxidiert.[3]
Einzelnachweise
Bearbeiten- ↑ a b c Datenblatt L-Histidinol-dihydrochlorid bei Sigma-Aldrich, abgerufen am 23. Dezember 2022 (PDF).
- ↑ Herbert Tabor: Methods in Enzymology. Band 3. Academic Press, 1957, [90] Isolation and determination of histidine and related compounds, S. 623–635, doi:10.1016/s0076-6879(57)03432-1.
- ↑ P Alifano, R Fani, P Liò, A Lazcano, M Bazzicalupo, M S Carlomagno, C B Bruni: Histidine biosynthetic pathway and genes: structure, regulation, and evolution. In: Microbiological Reviews. Band 60, Nr. 1, 1996, S. 44–69, doi:10.1128/mr.60.1.44-69.1996, PMID 8852895.
