Ammoniumhexafluorosilicat
Ammoniumhexafluorosilicat ist eine anorganische chemische Verbindung aus der Gruppe der Hexafluorosilicate.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 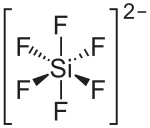
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Ammoniumhexafluorosilicat | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | (NH4)2[SiF6] | |||||||||||||||
| Kurzbeschreibung |
farbloser bis weißer Feststoff[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 178,15 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Dichte |
2,01 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
leicht in Wasser (186 g·l−1 bei 17 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Vorkommen Bearbeiten
Ammoniumhexafluorosilicat kommt natürlich in Form der Minerale Bararit und Cryptohalit vor.
Gewinnung und Darstellung Bearbeiten
Ammoniumhexafluorosilicat kann durch Reaktion von Hexafluorokieselsäure mit Ammoniak gewonnen werden.[5]
Eigenschaften Bearbeiten
Ammoniumhexafluorosilicat ist ein kristalliner, farbloser bis weißer Feststoff, der leicht löslich in Wasser ist. Er zersetzt sich bei Erhitzung über 145 °C, wobei Fluorwasserstoff und Siliciumtetrafluorid entstehen. Seine wässrige Lösung reagiert sauer.[2] Die Verbindung kommt in drei Modifikationen vor. Eine Form mit kubischer Kristallstruktur (Cryptohalit-Form) mit der Raumgruppe Fm3m (Raumgruppen-Nr. 225), eine Form mit trigonaler Kristallstruktur (Bararit-Form) mit der Raumgruppe P3m1 (Raumgruppen-Nr. 164) und eine Form mit hexagonaler Kristallstruktur mit der Raumgruppe P63mc (Raumgruppen-Nr. 186).[6][7] Die Cryptohalit Form wandelt sich unter Druck irreversibel in die Bararit-Form um.[8]
Verwendung Bearbeiten
Ammoniumhexafluorosilicat wird als Desinfektionsmittel und analytisches Reagens verwendet. Es findet auch Anwendung beim Ätzen von Glas, Metallguss und Galvanisierung und wird als Holzschutzmittel und Schmutzschutzmittel in Textilien eingesetzt. Es dient auch als Lötflussmittel und wird auch zur Kariesbehandlung ohne Verfärbung von demineralisiertem Zahnschmelz eingesetzt.[9][10]
Einzelnachweise Bearbeiten
- ↑ Eintrag zu AMMONIUM FLUOROSILICATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 1. Oktober 2021.
- ↑ a b c d e f g Eintrag zu Ammoniumhexafluorosilikat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ Datenblatt Ammonium Silicofluoride bei chemicalland21.com.
- ↑ Eintrag zu alkalifluorosilicates(NH4) im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 27. November 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Eintrag zu AMMONIUM SILICOFLUORIDE in der Hazardous Substances Data Bank (via PubChem), abgerufen am 25. November 2016.
- ↑ Pierre Villars, Karin Cenzual, Roman Gladyshevskii: Handbook. Walter de Gruyter GmbH & Co KG, 2015, ISBN 978-3-11-031174-7, S. 1081 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Bodie Douglas, Shi-Ming Ho: Structure and Chemistry of Crystalline Solids. Springer Science & Business Media, 2007, ISBN 978-0-387-36687-6, S. 111 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Elena V. Boldyreva, Tatyana P. Shakhtshneider, Heidrun Sowa, Hans Ahsbahs: Effect of hydrostatic pressure up to 6 GPa on the crystal structures of ammonium and sodium hexafluorosilicates, (NH4)2SiF6 and Na2SiF6; a phase transition in (NH4)2SiF6 at 0.2–0.3 GPa. In: Zeitschrift für Kristallographie, 2007, Band 222, Heft 1, S. 23–29, doi:10.1524/zkri.2007.222.1.23.
- ↑ Datenblatt Ammonium hexafluorosilicate, 99.999% (metals basis) bei Alfa Aesar, abgerufen am 25. November 2016 (Seite nicht mehr abrufbar).
- ↑ Y. Hosoya, E. Watanabe, K. Tadokoro, T. Inoue, M. Miyazaki, F. R. Tay: Effects of ammonium hexafluorosilicate application on demineralized enamel and dentin of primary teeth. In: Journal of oral science. Band 54, Nummer 3, September 2012, S. 267–272, PMID 23047038.
