Calciumbromid ist das Calciumsalz der Bromwasserstoffsäure (Bromide). Es ist ein farbloser, an der Luft sich langsam gelb färbender Feststoff.
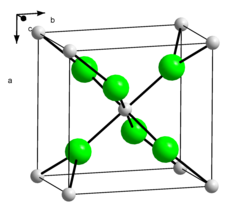
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| _ Ca2+ _ Br− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Calciumbromid | ||||||||||||||||||
| Andere Namen |
Calciumdibromid | ||||||||||||||||||
| Verhältnisformel | CaBr2 | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 199,88 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt |
730 °C[2] | ||||||||||||||||||
| Siedepunkt |
806–812 °C[2] | ||||||||||||||||||
| Löslichkeit |
gut in Wasser (1420 g·l−1 bei 20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Gewinnung und Darstellung
BearbeitenCalciumbromid lässt sich durch Reaktion von Calciumcarbonat, Calciumoxid oder Calciumhydroxid mit Bromwasserstoff gewinnen.[3]
Eine Alternative ist die Umsetzung der Calciumsalze mit Brom und einem Reduktionsmittel wie Ameisensäure oder Formaldehyd.[3]
Eigenschaften
BearbeitenCalciumbromid kristallisiert wie Calciumchlorid und Strontiumchlorid in der Calciumchloridstruktur, die der Rutilstruktur ähnlich ist. Im gasförmigen Zustand bildet es lineare Moleküle.[5] Es ist auch ein kristallines Hexahydrat bekannt, das trigonal in der Raumgruppe P321 (Raumgruppen-Nr. 150) mit den Gitterparametern a = 8,164 Å und c = 4,016 Å kristallisiert.[6]
An der Luft färbt sich die Verbindung langsam gelb, da sich elementares Brom bildet. Calciumbromid ist in Wasser und Methanol gut, in Ether und Chloroform nur in geringem Maß löslich.[7]
Verwendung
BearbeitenCalciumbromid wird zur Herstellung von Photoplatten, als Arzneimittel, in Holzschutz- sowie in Flammschutzmitteln eingesetzt.[3]
Einzelnachweise
Bearbeiten- ↑ Datenblatt Calciumbromid bei Sigma-Aldrich, abgerufen am 15. März 2011 (PDF).
- ↑ a b c d Datenblatt Calciumbromid bei Alfa Aesar, abgerufen am 9. Juni 2009 (Seite nicht mehr abrufbar).
- ↑ a b c d e Yoffe, D.; Frim, R.; Ukeles, S.D.; Dagani, M.J.; Barda, H.J.; Benya, T.J.; Sanders, D.C.: Bromine Compounds, in: Ullmanns Enzyklopädie der Technischen Chemie, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2013; doi:10.1002/14356007.a04_405.pub2.
- ↑ a b Eintrag zu Calciumbromid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1241.
- ↑ A. Leclaire, M.M. Borel: Le dichlorure et le dibromure de calcium hexahydrates. In: Acta Crystallographica, B33, 1977, S. 2938–2940, doi:10.1107/S0567740877009881.
- ↑ Eintrag zu Calciumbromid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 3. Januar 2015.
