Hexatriacontan ist ein langkettiges, unverzweigtes und gesättigtes Alkan. Es gehört dabei zur Gruppe der höheren Alkane.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
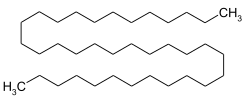
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Hexatriacontan | |||||||||||||||
| Andere Namen |
n-Hexatriacontan | |||||||||||||||
| Summenformel | C36H74 | |||||||||||||||
| Kurzbeschreibung | ||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 506,97 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte | ||||||||||||||||
| Schmelzpunkt |
76 °C[4] | |||||||||||||||
| Siedepunkt |
497 °C[2] | |||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[2] | |||||||||||||||
| Brechungsindex |
1,4397 (80 °C)[5] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Darstellung und Gewinnung
BearbeitenEine Herstellung gelingt durch die Wurtzsche Synthese aus Octadecyliodid und Natrium.[6]
Eigenschaften
BearbeitenHexatriacontan tritt in drei polymorphen Kristallformen auf.[4][7][1] Die Form I schmilzt bei 76 °C mit einer Schmelzenthalpie von 88,74 kJ·mol−1.[8] Dem Schmelzpunkt sind zwei Festphasenübergänge vorgelagert. Bei 72 °C erfolgt die Umwandlung der Form III zur Form II, bei 74 °C die Umwandlung von Form II zu Form I.[4][7][1] Bei Raumtemperatur ist die Kristallform III die thermodynamisch stabile Form. Die Verbindung kann in monoklinen Kristallgittern für die Formen II und III[9] und einem orthorhombischen[3][10] Kristallgitter für Form I auftreten.[11][12]
Die Dampfdruckkurve lässt sich im Temperaturbereich von 452 K bis 516 K mit der August-Gleichung als log10(p) = A−(B/T) (p in kPa, T in K) mit A = 14,67 und B = 8228 beschreiben.[13] Die Verdampfungsenthalpie beträgt 157 kJ·mol−1.[13]
Die Verbindung ist mit Heptan unbegrenzt mischbar. Die Löslichkeitskurve zeigt bei niedrigen Temperaturen nur einen geringen Gehalt an Hexatriacontan, der mit steigender Temperatur sehr schnell ansteigt.[8]
Verwendung
BearbeitenHexatriacontan wird als Standard in der Festkörper-NMR-Spektroskopie eingesetzt.[14]
Einzelnachweise
Bearbeiten- ↑ a b c Lan Wang, Zhi-Cheng Tan, Shuang-He Meng, Dong-Bai Liang: Low-temperature heat capacity and phase transition of n-hexatriacontane. In: Thermochim. Acta. 342, 1999, S. 59–65. doi:10.1016/S0040-6031(99)00308-1
- ↑ a b c d e Datenblatt n-Hexatriacontan bei Alfa Aesar, abgerufen am 24. Februar 2012 (Seite nicht mehr abrufbar).
- ↑ a b c V. Vand: Density and Unit Cell of n-Hexatriacontane. In: Acta Cryst. 6, 1953, S. 797–798. doi:10.1107/S0365110X53002246
- ↑ a b c J. C. Company: Measurement and interpretation of crystallization equilibriums of heavy paraffin and aromatic hydrocarbon solutions. In: Chem. Eng. Sci. 28, 1973, S. 318–323. doi:10.1016/0009-2509(73)85117-6
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-282.
- ↑ R. K. Doolittle, R. H. Peterson: Preparation and Physical Properties of a Series of n-Alkanes. In: J. Am. Chem. Soc. 73, 1951, S. 2145–2149. doi:10.1021/ja01149a069
- ↑ a b A. A. Schaerer, C. J. Busso, A. E. Smith, L. B. Skinner: Properties of pure normal alkanes in the C17 to C36 range. In: J. Am. Chem. Soc. 77, 1955, S. 2017–2019. doi:10.1021/ja01612a097
- ↑ a b K. L. Roberts, R. W. Rousseau, A. S. Teja: Solubility of Long-Chain n-Alkanes in Heptane between 280 and 350 K. In: J. Chem. Eng. Data. 39, 1994, S. 793–795. doi:10.1021/je00016a035
- ↑ H. M. M. Shearer, V. Vand: The crystal structure of the monoclinic form of n-hexatriacontane. In: Acta Cryst. 9, 1956, S. 379–384. doi:10.1107/S0365110X5600111X
- ↑ P. W. Teare: The crystal structure of orthorhombic hexatriacontane, C36H74. In: Acta Cryst. 12, 1959, S. 294–300. doi:10.1107/S0365110X59000901
- ↑ Hidehiko Honda, Hiroshi Ogura, Shuichi Tasaki, Akio Chiba: Two-phase coexisting state of n-hexatriacontane in the first-order phase transition. In: Thermochim. Acta. 405, 2003, S. 51–60. doi:10.1016/S0040-6031(03)00135-7
- ↑ Hideki Kubota, Fumitoshi Kaneko, Tatsuya Kawaguchi, Masatsugu Kawasaki: Infrared spectroscopic study on polytypic transformation of growing single crystal of n-hexatriacontane n-C36H74. In: J. Cryst. Growth. 275, 2005, S. e1751–e1756. doi:10.1016/j.jcrysgro.2004.11.163
- ↑ a b V. Piacente, D. Fontana, P. Scardala: Enthalpies of Vaporization of a Homologous Series of n-Alkanes Determined from Vapor Pressure Measurements. In: J. Chem. Eng. Data. 39, 1994, S. 231–237. doi:10.1021/je00014a009
- ↑ Hideki Kubota, Fumitoshi Kaneko, Chikayo Akita, Tatsuya Kawaguchi: The Influence of Polytropic Structures on the Solid-state 13C NMR Spectra of n-Alkanes. In: Chem. Lett. 33, 2004, S. 1358–1359. doi:10.1246/cl.2004.1358