Canakinumab
Canakinumab (Handelsname Ilaris; Hersteller Novartis) ist ein Arzneistoff, der zur Behandlung periodischer Fiebersyndrome, der Gichtarthritis sowie des Still-Syndroms einschließlich der systemischen juvenilen idiopathischen Arthritis (sJIA) eingesetzt wird. Es handelt sich um einen humanen, monoklonalen Antikörper gegen Interleukin-1β (IL-1β). Interleukin-1β ist ein Zytokin, welches im menschlichen Körper Entzündungsreaktionen reguliert.[1]
| Canakinumab | ||
|---|---|---|
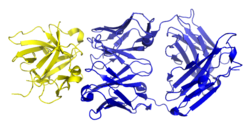
| ||
| Bändermodell von Canakinumab (blau) gebunden an IL-1β (gelb), nach PDB 5BVP | ||
| Andere Namen |
ACZ-885 | |
|
Vorhandene Strukturdaten: 5BVP | ||
| Masse/Länge Primärstruktur | 1322–1324 Aminosäuren, 145.157 Da | |
| Bezeichner | ||
| Externe IDs | ||
| Arzneistoffangaben | ||
| ATC-Code | L04AC08 | |
| DrugBank | DB06168 | |
| Wirkstoffklasse | Interleukin-1β-Inhibitor | |
Applikationsform und Dosierung
BearbeitenCanakinumab wird als subkutane Injektion verabreicht. Die Dosierung von Canakinumab ist sehr vielfältig aufgrund der Vielfalt an Krankheiten, welche damit behandelt werden können. Normalerweise liegt die Dosierung bei 2 mg/kg und 4 mg/kg und die maximale Dosis bei 300 mg (Morbus Still) oder 600 mg (periodische Fiebersyndrome). Eine Injektionslösung enthält 150 mg Canakinumab.[1]
Klinische Angaben
BearbeitenStill-Syndrom
BearbeitenCanakinumab ist zur Behandlung des Still-Syndroms (Morbus Still) einschließlich des adulten Still-Syndroms (adult-onset Still’s disease; AOSD) und der systemischen juvenilen idiopathischen Arthritis (sJIA) ab dem 2. Lebensjahr zugelassen.[1] Beim Still-Syndrom gibt es zwei vom Hersteller vorgeschlagene Therapiemöglichkeiten:
- eine Monotherapie[1]
- eine Kombinationstherapie mit Methotrexat[1]
Canakinumab blockiert den Interleukin-1β-Rezeptor und reduziert dadurch bestimmte Entzündungsreaktionen im Körper. Somit wird die zugrunde liegende Krankheit bekämpft und entsprechende Blutwerte wie beispielsweise der CRP-Wert sinken wieder in den Normalbereich. Der Hersteller, Novartis, empfiehlt eine Dosierung ab einem Körpergewicht von 7,5 kg, von 4 mg/kg. Diese soll alle vier Wochen in Form einer subkutanen Injektion durch einen Arzt erfolgen. Die maximale Dosis liegt hier bei 300 mg. Sollte hierbei keine Verbesserung erfolgen, so ist von einer weiteren Canakinumab-Behandlung abzusehen.
Periodische Fiebersyndrome
BearbeitenNeben rheumatischen Erkrankungen ist Canakinumab ebenfalls für die folgenden periodischen Fiebersyndrome eine Behandlungsmöglichkeit:
Cryopyrinassozierte periodische Syndrome
BearbeitenBei Cryopyrin-assoziiertes periodisches Syndrom (CAPS) ist Canakinumab ab dem 2. Lebensjahr zugelassen. Hier werden zunächst 150 mg oder 2 mg/kg, je nach Körpergewicht, als Anfangsdosis appliziert.[1] Sollte nach sieben Tagen kein Fortschritt erfolgt sein, sollte eine zweite Injektion mit derselben Dosierung in Erwägung gezogen werden.[1]
Sollte dies Erfolg haben, sollte alle acht Wochen mit 300 mg bzw. 4 mg/kg eine nächste Injektion erfolgen.
TRAPS, MKD/HIDS, FMF
BearbeitenAußerdem ist Canakinumab für Tumor-Nekrose-Faktor-Rezeptor-assoziiertes periodisches Syndrom (TRAPS), Hyperimmunglobulin-D-Syndrom (HIDS), Mevalonatkinase-Defizienz (MKD) und dem Familiären Mittelmeerfieber (FMF) zugelassen.[1] Auch hier empfiehlt Novartis verschiedene Anfangsdosierungen:
- Sollte der Patient mehr als 40 kg wiegen, beträgt die empfohlene Anfangsdosis 150 mg.[1]
- Sollte der Patient zwischen 7,5 kg und 40 kg wiegen, empfiehlt der Hersteller 2 mg/kg.[1]
Genauso wie bei der sJIA wird hier eine einzelne subkutane Injektion alle vier Wochen verabreicht.
Gichtarthritis
BearbeitenBei Gichtarthritis wird Canakinumab zu einer symptomatischen Behandlung bei erwachsenen Patienten mit häufigen Gichtanfällen (mindestens drei in den letzten zwölf Monaten) angewendet.[1] Canakinumab wird hier jedoch nur appliziert, wenn nichtsteroidale Antirheumatika (NSAR) und Colchicin kontraindiziert oder unverträglich sind.[1] Außerdem kann Canakinumab bei einem starken Gichtanfall angewendet werden, wenn nach wiederholten Kortison-Zyklen keine Verbesserung erkennbar ist.[1]
Nebenwirkungen
BearbeitenIn der Regel wird Canakinumab gut vertragen. Mögliche Nebenwirkungen sind:
- Rötung an der Injektionsstelle
- Juckreiz
- Schwindel
- Infektion der oberen Atemwege
Wechselwirkungen
BearbeitenBisher (Stand 2017) wurden keine Wechselwirkungen mit anderen Medikamenten festgestellt.[2] Trotzdem sollte Canakinumab nicht in Kombination mit anderen Biologika verabreicht werden.[2]
Schwangerschaft und Stillzeit
BearbeitenDie Datenverfügbarkeit von schwangeren Canakinumab-Patientinnen ist sehr begrenzt.[1] Hier schlägt der Hersteller eine gründliche Nutzen-Risiko-Abwägung durch den behandelten Arzt vor. Trotzdem wird empfohlen, Neugeborenen erst 16 Wochen nach der Geburt Lebendimpfstoffe zu verabreichen.[1]
Einzelnachweise
Bearbeiten- ↑ a b c d e f g h i j k l m n o Novartis Pharma: Ilaris – Fachinformation 150 mg/ml Injektionslösung. In: Ilaris® (Canakinumab) – Informationen zur sicheren Anwendung. Novartis Pharma, 1. Juli 2019, abgerufen am 3. Februar 2020.
- ↑ a b Behandlung mit Canakinumab. Deutsche Gesellschaft für Rheumatologie e.v., 1. Juni 2017, abgerufen am 9. Februar 2020.