Triglycinsulfat
Triglycinsulfat (TGS) kann formal als Addukt von drei Mol Glycin und einem Mol Schwefelsäure aufgefasst werden. TGS-Einkristalle werden als Detektormaterial in pyroelektrischen Sensoren verwendet.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
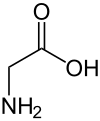 
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Triglycinsulfat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H17N3O10S | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 323,28 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
1,69 g·cm−3[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Anwendung Bearbeiten
Triglycinsulfat ist ein Ferroelektrikum und besitzt einen großen pyroelektrischen Koeffizienten. Erfolgt eine Temperaturänderung, beispielsweise durch Absorption elektromagnetischer Wellen, ändert sich die Polarisation und es wird eine Ladungserzeugung bewirkt, die nach Verstärkung unmittelbar messbar ist. Dazu müssen die jeweiligen Einkristallflächen mit geeigneten Elektroden versehen sein. Mit einer ähnlichen Anordnung sind auch Temperaturen messbar.[3] Die Curie-Temperatur von TGS beträgt 49 °C.[4] Unterhalb dieser Temperatur ändert sich die Polarisation bei Änderung der auftreffenden Strahlungsleistung, was in Form eines Spannungsstoßes messbar wird.
Deuteriertes Triglycinsulfat Bearbeiten
Deuteriertes Triglycinsulfat (DTGS) unterscheidet sich von TGS durch eine vollständige Substitution aller Wasserstoffatome durch Deuteriumatome. Die Summenformel lautet C6D17N3SO10. DTGS hat die CAS-Nr. 17237-73-9 und besitzt als kristalliner Feststoff die molare Masse 340,18 g·mol−1.
Auch DTGS weist pyroelektrische Eigenschaften auf. Es hat gegenüber TGS den Vorteil einer höheren Curie-Temperatur, diese liegt abhängig vom Grad der Deuterierung bei 57–62 °C,[4] statt 49 °C bei TGS. Der Unterschied in der Curie-Temperatur hat einen großen Einfluss auf die Anwendungsbereiche von DTGS-basierten Sensoren. Beispielsweise kann bereits direkte Sonneneinstrahlung einen Sensor auf 50 °C erwärmen. Oberhalb der Curie-Temperatur gehen jedoch die pyroelektrischen Eigenschaften verloren und der Detektor verliert seine Funktion. DTGS-Sensoren bieten daher einen größeren Anwendungsbereich als TGS-Detektoren, vor allem im Fall eines passiv gekühlten Betriebs.
Eine weitere Verbesserung der pyroelektrischen Eigenschaften ist durch eine Dotierung der DTGS-Kristalle mit L-Alanin erreichbar, sogenanntes deuteriertes L-Alanin dotiertes Triglycinsulfat (DLaTGS). Durch die Alanindotierung kann zum einen die Empfindlichkeit der DTGS-Kristalle erhöht zum anderen die dauerhafte Depolarisation bei Erwärmungen über die Curie-Temperatur reduziert werden.
DTGS und DLaTGS haben aufgrund ihrer Stoffeigenschaften Bedeutung als Sensormaterial bei der Infrarotspektroskopie erlangt.[5]
Einzelnachweise Bearbeiten
- ↑ a b c d Eintrag zu GlycineSulfate, >98.0% bei TCI Europe, abgerufen am 16. Oktober 2023.
- ↑ E. A. Wood, A. N. Holden: Monoclinic glycine sulfate: crystallographic data. In: Acta Cryst. 1957, 10, S. 145–146, doi:10.1107/S0365110X57000481.
- ↑ Patent EP0011808: Pyroelektrisches Bauelement für die Messung der Intensität elektromagnetischer Strahlung, für die Temperaturmessung sowie für die thermoelektrische Stromerzeugung und Verwendung dieses Bauelements. Erfinder: Siegfried Haussühl, Josef Liebertz (Beschreibung von TGS in den Punkten 0002 und 0003).
- ↑ a b Triglycine sulfate (TGS) & Deuterated triglycine sulfate (DTGS) (Memento vom 24. November 2009 im Internet Archive). GIRMET Ltd.
- ↑ DTGS-Detektoren im Lexikon der IR-Spektroskopie