Ethylendiamindibernsteinsäure
Ethylendiamindibernsteinsäure (Ethylendiamindisuccinat, abgekürzt mit EDDS) ist als mehrzähniger Ligand ein Chelatkomplex-Bildner. Es hat eine ähnliche chemische Struktur und auch ähnliche Eigenschaften wie EDTA.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
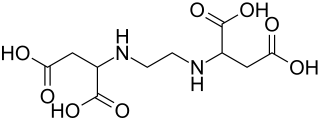
| |||||||||||||
| Strukturformel ohne Stereochemie | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Ethylendiamindibernsteinsäure | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C10H16N2O8 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 292,24 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Schmelzpunkt |
147–149 °C (S,S-Form)[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Isomerie Bearbeiten
Ethylendiamindibernsteinsäure besitzt zwei Stereozentren, so dass es in drei verschiedenen Stereoisomeren auftritt:
- (S,S)-EDDS,
- (R,R)-EDDS und
- meso-EDDS [(R,S)-EDDS].
Vorkommen Bearbeiten
In verschiedene Actinomyceten kommt (S,S)-EDDS natürlich vor.
Gewinnung und Darstellung Bearbeiten
Ein einfacher, großindustriell leicht gangbarer Zugang zu EDDS stellt die Addition von Ethylendiamin an Maleinsäuremonobenzylester und der anschließenden Verseifung des Esters dar.[3] Allerdings erhält man auf diesem Weg ein Stereoisomerengemisch, welches zu gleichen Teilen aus den (S,S)- und dem (R,R)-Isomeren sowie außerdem dem (R,S)-Isomer (= meso-Form) besteht.
Eine gezielte, jedoch teurere Synthese für (S,S)-EDDS besteht in der Umsetzung von L-Asparaginsäure mit 1,2-Dibromethan.
Verwendung Bearbeiten
EDDS dient als Ersatz für EDTA. Die Komplexbildungskonstanten für die Chelatkomplexe mit Metallionen sind meist nur geringfügig kleiner als die des EDTA, so dass es dieses weitestgehend substituieren könnte. Die Anwendungsgebiete gleichen denen des EDTAs, z. B.
- Zusatz zu Reinigungsmitteln (Wasserenthärtung durch Bindung von Ca2+/Mg2+),
- Komplexierung von Schwermetallionen,
- Bodenwäsche schwermetallverseuchten Erdraums.
(S,S)-EDDS ist leicht vollständig biologisch abbaubar, meso-EDDS ist teilweise biologisch abbaubar; problematisch ist das (R,R)-Stereoisomer, welches in der Umwelt persistiert. Dennoch erscheint EDDS als zumindest teilweise biologisch abbaubarer Ersatz für das vergleichsweise äußerst langlebige EDTA. Das (S,S)-Stereoisomer ist ein Derivat der natürlichen Aminosäure L-Asparaginsäure [(S)-Asparaginsäure] – darin begründet sich auch die gute biologische Abbaubarkeit.[4][5][6]
Einzelnachweise Bearbeiten
- ↑ a b John Buckingham: Dictionary of Organic Compounds. Taylor & Francis, 1987, ISBN 978-0-412-17050-8, S. 316 (books.google.com).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Michel Barbier, Daria Bogdanovsky, Walter Vetter, Edgar Lederer: Synthese und Eigenschaften eines Analogen des Lycomarasmins und der Aspergillomarasmine. In: Justus Liebigs Annalen der Chemie. 668, 1963, S. 132, doi:10.1002/jlac.19636680115.
- ↑ D. Schowanek, T. C. Feijtel, C. M. Perkins, F. A. Hartman, T. W. Federle, R. J. Larson: Biodegradation of [S,S], [R,R] and mixed stereoisomers of ethylene diamine disuccinic acid (EDDS), a transition metal chelator. In: Chemosphere Band 34, Nummer 11, Juni 1997, S. 2375–2391, PMID 9192467.
- ↑ P. C. Vandevivere, H. Saveyn, W. Verstraete, T. C. Feijtel, D. R. Schowanek: Biodegradation of metal-[S,S]-EDDS complexes. In: Environmental Science & Technology Band 35, Nummer 9, Mai 2001, S. 1765–1770, PMID 11355190.
- ↑ T. C. Yip, D. C. Tsang, K. T. Ng, I. M. Lo: Kinetic interactions of EDDS with soils. 1. Metal resorption and competition under EDDS deficiency. In: Environmental Science & Technology Band 43, Nummer 3, Februar 2009, S. 831–836, PMID 19245023.