Kohlensäureester
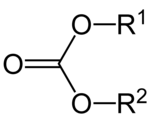
Kohlensäureester (häufig auch ungenau Carbonate genannt) sind die Ester der in Substanz instabilen Kohlensäure. Ihre allgemeine Halbstrukturformel ist R1–O–C(=O)–O–R2, wobei R1 und R2 kohlenstoffhaltige Alkyl- oder Arylreste sind. Im Fall R1= R2 ist der Kohlensäureester symmetrisch, bei R1≠ R2 ist der Kohlensäureester unsymmetrisch. Gehören R1 und R2 zu demselben Molekül, so bildet sich eine ringförmige Verbindung wie beispielsweise Propylencarbonat. Ist die Kohlensäurefunktion auf einer Seite unfunktionalisiert (R = H), so spricht man von einem Halbester. Die Urethane können ebenfalls als Halbester der Kohlensäure klassifiziert werden, zugleich sind sie Halbamide der Kohlensäure.
Herstellung Bearbeiten
Kohlensäureester können aus Phosgen und Alkoholen unter Abspaltung von Chlorwasserstoff hergestellt werden:[1]
Mit 1,2-Glycolen entstehen die cyclischen Carbonate Ethylencarbonat und Propylencarbonat nur als Nebenprodukte neben Polycarbonaten.
Verwendung Bearbeiten
Kohlensäureester zeigen als recht polare Lösungsmittel eine gewisse Löslichkeit von anorganischen Salzen und werden daher als Elektrolytflüssigkeit (Li-Ionen-Akkus) verwendet. Besonders bekannte Kohlensäureester sind die Polycarbonate, die als Kunststoffe vielfältige Verwendung finden. Das sogenannte Triphosgen (Kohlensäure-bis-trichlormethylester) kann als weniger gefährlicher Ersatz für Phosgen in Synthesen verwendet werden.[2]
Weiteres Bearbeiten
Neben den Kohlensäureestern der allgemeinen Formel CO(OR)2 gibt es auch sogenannte Orthokohlensäureester C(OR)4 (siehe auch Orthoester). Diese können durch Reaktion von Chlorpikrin mit Alkoholaten erhalten werden:[2]
Beispiele Bearbeiten
Literatur Bearbeiten
- Benjamin Schäffner, Sergey P. Verevkin und Armin Börner: Organische Carbonate, Chem. Unserer Zeit 43 (2009) 12–21.
Einzelnachweise Bearbeiten
- ↑ Eintrag zu Kohlensäureester. In: Römpp Online. Georg Thieme Verlag, abgerufen am 16. Juni 2014.
- ↑ a b Beyer, Walter: Lehrbuch der Organischen Chemie, 23. Auflage, S. Hirzel Verlag 1998.