Rotenon
Rotenon ist ein isoflavonoides Benzopyrano-Furochroman-4-on-Derivat.[6][7] Es ist der bekannteste Vertreter der Rotenoide. Rotenon ist weit verbreitet in der Familie der Fabaceae, z. B. in der Tubawurzel (Derris elliptica), Pachyrhizus erosus, sowie in Lonchocarpus-Arten und Tephrosia-Arten. Rotenon findet Verwendung als Insektizid und Akarizid, ist jedoch auch für Fische sehr giftig (weniger giftig für Säugetiere und Bienen) und wird deshalb traditionell als Wirkstoff des Barbasco im Fischfang verwendet.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
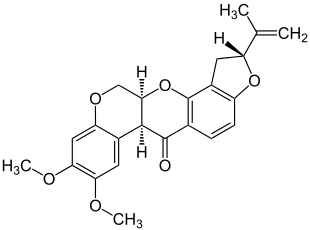
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Rotenon | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C23H22O6 | |||||||||||||||||||||
| Kurzbeschreibung |
kristalline, orthorhombische Platten[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 394,42 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
in Wasser unlöslich, in Ethanol, Benzol, Aceton gut, in Chloroform sehr gut löslich[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
Schweiz: 5 mg·m−3 (gemessen als einatembarer Staub)[4] | |||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Herkunft Bearbeiten
Rotenon wird unter anderem aus der Wurzel von Deguelia utilis oder der Tubawurzel (Derris elliptica), einem in Borneo heimischen Schmetterlingsblütler, gewonnen. Die Wirkung dieser Pflanzen (und damit des Giftes) war schon seit dem 17. Jahrhundert bekannt.
Wirkung Bearbeiten
Die giftige Wirkung des Stoffes beruht auf einer Blockade der an der inneren Membran der Mitochondrien lokalisierten Atmungskette, wo er am Komplex I ansetzt und so die Elektronenübertragung verhindert. Dadurch kann die Zelle kein ATP mehr herstellen und der Stoffwechsel kommt schließlich zum Erliegen. Nicht nur die Fischer der Trobriand-Inseln machten sich diese Eigenschaft beim Fischfang zunutze – mit dem Rotenon aus zerstampften Derriswurzeln wurden Fische betäubt und anschließend aufgespießt. Auch in Mexiko, Ecuador und Brasilien findet die Pflanze als Barbasco Anwendung im Fischfang.
Im Freien zersetzt sich Rotenon relativ schnell, ist aber dennoch gefährlich, da es auch über die Haut oder als Staub in die Lunge eindringen kann. Laut einigen Studien steht Rotenon in Verdacht, Parkinson-Krankheit auszulösen.[8] Die Technische Universität Dresden wies die auslösende und verstärkende Wirkung von Rotenon auf das Protein Alpha-Synuclein im Darm bei Mäusen nach, welches Ursache mancher Parkinsonarten ist.[9] Einige der Tiere zeigten Gewebeveränderungen im Gehirn, die denen ähnlich sind, die man bei Parkinson-Patienten findet.
Einsatzgebiet Bearbeiten
Rotenon ist weder in den Staaten der EU noch in der Schweiz als Insektizid zugelassen, es befinden sich keine Pflanzenschutzmittel mit Rotenon als Wirkstoff im Handel.[10]
In Norwegen wird Rotenon erfolgreich eingesetzt, um einen Parasiten (Gyrodactylus salaris), der den Lachsbestand in einigen Flüssen bedroht, zu bekämpfen.[11] Ursprünglich waren 50 norwegische Flüsse mit dem Parasiten infiziert – heute (Stand: Dezember 2016) ist der Parasit nur noch in sieben Flüssen zu finden.[12][13] Bei solchen Behandlungen wird nicht der Parasit getötet, sondern der Wirt – in diesem Falle also alle lachsartigen Fische (in Norwegen sind das Lachse, Forellen und Saiblinge). Rotenon wird allerdings nicht nur in Norwegen eingesetzt, sondern auch z. B. in Großbritannien, Spanien, den USA und Afrika.[14][15][16][17][18] In diesen Ländern benutzt man Rotenon hauptsächlich, um eingeführte/invasive Fischarten auszurotten und deren Ausbreitung zu unterbinden. Nach einer durchgeführten Rotenonbehandlung müssen diese Gewässer wieder mit neuen Fischbeständen besetzt werden.
Literatur Bearbeiten
- Burkhard Fugmann: Römpp-Lexikon Naturstoffe; Thieme, New York, 1997
- M. Wink: Handbuch der giftigen und psychoaktiven Pflanzen; Wissensch. Verlagsg. mbH 2008
Weblinks Bearbeiten
Einzelnachweise Bearbeiten
- ↑ a b c d e Eintrag zu Rotenon. In: Römpp Online. Georg Thieme Verlag, abgerufen am 7. Februar 2014.
- ↑ a b Eintrag zu Rotenon in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ Eintrag zu (2R,6aS,12aS)-1,2,6,6a,12,12a-hexahydro-2-isopropenyl-8,9-dimethoxychromeno[3,4-b]furo[2,3-h]chromen-6-one im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 83-79-4 bzw. Rotenon), abgerufen am 2. November 2015.
- ↑ Down to Earth. 35(25), 1979.
- ↑ Eintrag zu Rotenon. In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. März 2021.
- ↑ The Shikimate Pathway: Aromatic Amino Acids and Phenylpropanoids. In: Medicinal Natural Products. John Wiley & Sons, Ltd, 2009, ISBN 978-0-470-74276-1, S. 137–186, doi:10.1002/9780470742761.ch4.
- ↑ Pflanzenschutzmittel können Parkinson auslösen. In: Die Welt. 5. Dezember 2012. Aufgerufen am 5. Dezember 2012.
- ↑ Francisco Pan-Montojo, Mathias Schwarz, Clemens Winkler, Mike Arnhold, Gregory A. O’Sullivan, Arun Pal, Jonas Said, Giovanni Marsico, Jean-Marc Verbavatz, Margarita Rodrigo-Angulo, Gabriele Gille, Richard H. W. Funk & Heinz Reichmann: Environmental toxins trigger PD-like progression via increased alpha-synuclein release from enteric neurons in mice. In: Scientific Reports. 2, 2012, doi:10.1038/srep00898.
- ↑ Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Rotenone in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs und Deutschlands, abgerufen am 3. Februar 2018.
- ↑ Gyrodactylus salaris. In: www.miljødirektoratet.no. Abgerufen am 2. Januar 2017.
- ↑ Regioner infisert av Gyrodactylus salaris. In: www.miljødirektoratet.no. Abgerufen am 2. Januar 2017.
- ↑ Friskmeldte vassdrag. In: www.xn--miljdirektoratet-oxb.no. Abgerufen am 2. Januar 2017.
- ↑ Marie Løvoll: Veso | Restoration and Eradication. In: www.veso.no. Abgerufen am 2. Januar 2017.
- ↑ Matthew S. Recsetar, Scott A. Bonar: Effectiveness of Two Commercial Rotenone Formulations in the Eradication of Virile Crayfish Orconectes virilis. In: North American Journal of Fisheries Management. Band 35, Nr. 3, 4. Mai 2015, S. 616–620, doi:10.1080/02755947.2015.1017127.
- ↑ Channa argus argus (northern snakehead). In: www.cabi.org. Abgerufen am 2. Januar 2017.
- ↑ Olaf L. F. Weyl, Brian Finlayson, N. Dean Impson, Darragh J. Woodford, Jarle Steinkjer: Threatened Endemic Fishes in South Africa's Cape Floristic Region: A New Beginning for the Rondegat River. In: Fisheries. Band 39, Nr. 6, 3. Juni 2014, S. 270–279, doi:10.1080/03632415.2014.914924.
- ↑ Manuel Ferreras-Romero, Joaquín Márquez-Rodríguez, Carlos Fernández-Delgado: Long-time effect of an invasive fish on the Odonata assemblage in a Mediterranean lake and early response after rotenone treatment. In: ResearchGate. Band 45, Nr. 1/2, 1. Juni 2016, doi:10.5281/zenodo.50846 (researchgate.net [abgerufen am 2. Januar 2017]).

